осторожно! вас хотят поиметь!
-
 Андрей Эдельвейсс
Андрей Эдельвейсс
Автор темы - Трактирщик
- Сообщения: 8358
- Зарегистрирован: 29 май 2015, 19:55
- Награды: 5
- Откуда: СССР
- Род занятий: колымим
- :




- Благодарил (а): 1099 раз
- Поблагодарили: 2392 раза
- Status: Не в сети

Разнотрав от давления: отзыв врача, цена, где купить
Комментариев (29)15 января 2018 Разделы: Товары для здоровья
raznotrav ot gipertoniiОказывается, в XVIII веке люди уже умели бороться с проявлениями артериальной гипертензии. Препаратов тогда еще не был. Использовались лекарственные растения. И сегодня эти старинные рецепты могут послужить во благо вашего здоровья. Каждый желающий может приобрести в интернете БАД под названием Разнотрав. Это средство обещает снизить артериальное давление раз и навсегда.
Средство от повышенного давления
Разнотрав не только нормализует давление, но еще оказывает ряд дополнительных клинических эффектов. Вот основные из них:
снижает уровень холестерина;
очищает сосуды от холестериновых бляшек, излечивая таким образом атеросклероз;
устраняет причины гипертонии, из-за чего давление снижается навсегда;
уменьшает риск инфаркта или инсульта на 96%;
снимает боль в сердце;
нормализует ритм сердца;
повышает сосудистый тонус;
очищает кровь;
уменьшает уровень сахара в крови.
Разнотрав показания
По мнению продавцов Разнотрава, сосуды нужно чистить постоянно, подобно тому, как мы чистим зубы по утрам. А иначе они потеряют эластичность и будут закупорены холестериновыми бляшками.
Обозначенный механизм действия:
Разнотрав насыщает кровь полезными веществами.
Эти полезные вещества стимулируют выработку определенного фермента (какого – не указано).
Безымянный фермент очищает сосуды от холестерина, жиров, и полностью растворяет бляшки.
Предполагается, что всего за 2 месяца приема Разнотрава можно полностью восстановить сердечно-сосудистую систему.
Инструкция по применению
1 чайную ложку порошка следует развести в половине стакана воды. Она должна быть комнатной температуры. Далее следует перемешать средство до полного растворения. После этого Разнотрав нужно выпить. Принимается порошок 2 раза в сутки. Интервалы между приемами не должны составлять меньше 6 часов. Если вы пропустили очередную дозу (забыли выпить Разнотрав), нельзя компенсировать этот пропуск, иначе возможна передозировка.
Состав
В составе Разнотрава содержатся такие растения:
гвоздика;
алоэ;
боярышник;
чага;
чеснок;
бессмертник;
семена тыквы;
пустырник.
Отзыв врача
Разнотрав не снизит ваше давление – это факт. БАД продается за счет голых, ничем не подкрепленных обещаний. Есть несколько причин считать это средство бесполезным:
БоярышникСостав. Разнотрав не содержит растений, которые способны оказать выраженное влияние на артериальное давление. Из всего списка трав можно отметить разве что боярышник и пустырник. Первый обладает кардиотоническими свойствами, второй имеет успокаивающее действие. Но если они и влияют на артериальное давление, то разве что в минимальной степени, снижают его на короткое время.
ПустырникЧрезмерное количество обещанных эффектов. Продавцы явно перестарались, щедро посыпая потенциального покупателя обещаниями. Разнотрав якобы и давление снижает, и холестерин понижает, и сердце лечит, и сахар в крови нормализует, и сон крепкий гарантирует… Только бабушку через дорогу не переводит, а всё остальное делает. Обычно подобные универсальные «всеисцеляющие» средства оказываются пустышками.
Нереальные эффекты. Продавцы Разнотрава утверждают, что риск инфаркта и инсульта после приема этого растительного комплекса уменьшается на 96%. Действительно, так бы оно и было, будь травяной сбор в действительности способен растворить в крови холестериновые бляшки. Но это невозможно. Медицина еще не достигла того уровня развития, чтобы прочищать кровеносные сосуды, восстанавливая их просвет.
Чистка сосудовНеясный механизм действия. Некий фермент (какой?) образуется под действием полезных веществ (каких?) и очищает сосуды от холестериновых бляшек. Полная несуразица. К тому же, продавцы при перечислении клинических эффектов утверждают, что у вас после приема Разнотрава повысится тонус сосудов. Но увеличение их тонуса привело бы к возрастанию, а не уменьшению артериального давления.
Учитывая плохой состав, противоречивую информацию о продукте на официальном сайте, а также неправдоподобные обещания, вряд ли Разнотрав стоит покупать как средство для лечения сердечных заболеваний и артериальной гипертензии.
Цена
Разнотрав стоит 147 рублей. На первый взгляд, это недорого. Но проблема в том, что цена указана не настоящая. Реальная стоимость продукта – 990 рублей. Именно такую цену вам озвучат, если вы свяжетесь с продавцами и начнете оформлять заказ. А за 147 рублей вам продадут только одну упаковку Разнотрава, лишь при условии, что две пачки порошка в купите по полной цене. Таким образом, вместе с доставкой и почтовым сбором курс лечения обойдется почти в 3 тысячи рублей.
Где купить?
Купить Разнотрав можно лишь в интернете. Продается он БАД официальном сайте. Доставка возможна только по России. Чтобы заказать продукт, нужно ввести личные данные в форму заказа. Затем кликнуть «Оформить заказ». Ожидайте – вам позвонит оператор с минуты на минуту. С ним вы обсудите все детали заказа. В случае его подтверждения на ваш адрес будет отправлена бандероль. Разнотрав заберете на почте через несколько дней.
Комментариев (29)15 января 2018 Разделы: Товары для здоровья
raznotrav ot gipertoniiОказывается, в XVIII веке люди уже умели бороться с проявлениями артериальной гипертензии. Препаратов тогда еще не был. Использовались лекарственные растения. И сегодня эти старинные рецепты могут послужить во благо вашего здоровья. Каждый желающий может приобрести в интернете БАД под названием Разнотрав. Это средство обещает снизить артериальное давление раз и навсегда.
Средство от повышенного давления
Разнотрав не только нормализует давление, но еще оказывает ряд дополнительных клинических эффектов. Вот основные из них:
снижает уровень холестерина;
очищает сосуды от холестериновых бляшек, излечивая таким образом атеросклероз;
устраняет причины гипертонии, из-за чего давление снижается навсегда;
уменьшает риск инфаркта или инсульта на 96%;
снимает боль в сердце;
нормализует ритм сердца;
повышает сосудистый тонус;
очищает кровь;
уменьшает уровень сахара в крови.
Разнотрав показания
По мнению продавцов Разнотрава, сосуды нужно чистить постоянно, подобно тому, как мы чистим зубы по утрам. А иначе они потеряют эластичность и будут закупорены холестериновыми бляшками.
Обозначенный механизм действия:
Разнотрав насыщает кровь полезными веществами.
Эти полезные вещества стимулируют выработку определенного фермента (какого – не указано).
Безымянный фермент очищает сосуды от холестерина, жиров, и полностью растворяет бляшки.
Предполагается, что всего за 2 месяца приема Разнотрава можно полностью восстановить сердечно-сосудистую систему.
Инструкция по применению
1 чайную ложку порошка следует развести в половине стакана воды. Она должна быть комнатной температуры. Далее следует перемешать средство до полного растворения. После этого Разнотрав нужно выпить. Принимается порошок 2 раза в сутки. Интервалы между приемами не должны составлять меньше 6 часов. Если вы пропустили очередную дозу (забыли выпить Разнотрав), нельзя компенсировать этот пропуск, иначе возможна передозировка.
Состав
В составе Разнотрава содержатся такие растения:
гвоздика;
алоэ;
боярышник;
чага;
чеснок;
бессмертник;
семена тыквы;
пустырник.
Отзыв врача
Разнотрав не снизит ваше давление – это факт. БАД продается за счет голых, ничем не подкрепленных обещаний. Есть несколько причин считать это средство бесполезным:
БоярышникСостав. Разнотрав не содержит растений, которые способны оказать выраженное влияние на артериальное давление. Из всего списка трав можно отметить разве что боярышник и пустырник. Первый обладает кардиотоническими свойствами, второй имеет успокаивающее действие. Но если они и влияют на артериальное давление, то разве что в минимальной степени, снижают его на короткое время.
ПустырникЧрезмерное количество обещанных эффектов. Продавцы явно перестарались, щедро посыпая потенциального покупателя обещаниями. Разнотрав якобы и давление снижает, и холестерин понижает, и сердце лечит, и сахар в крови нормализует, и сон крепкий гарантирует… Только бабушку через дорогу не переводит, а всё остальное делает. Обычно подобные универсальные «всеисцеляющие» средства оказываются пустышками.
Нереальные эффекты. Продавцы Разнотрава утверждают, что риск инфаркта и инсульта после приема этого растительного комплекса уменьшается на 96%. Действительно, так бы оно и было, будь травяной сбор в действительности способен растворить в крови холестериновые бляшки. Но это невозможно. Медицина еще не достигла того уровня развития, чтобы прочищать кровеносные сосуды, восстанавливая их просвет.
Чистка сосудовНеясный механизм действия. Некий фермент (какой?) образуется под действием полезных веществ (каких?) и очищает сосуды от холестериновых бляшек. Полная несуразица. К тому же, продавцы при перечислении клинических эффектов утверждают, что у вас после приема Разнотрава повысится тонус сосудов. Но увеличение их тонуса привело бы к возрастанию, а не уменьшению артериального давления.
Учитывая плохой состав, противоречивую информацию о продукте на официальном сайте, а также неправдоподобные обещания, вряд ли Разнотрав стоит покупать как средство для лечения сердечных заболеваний и артериальной гипертензии.
Цена
Разнотрав стоит 147 рублей. На первый взгляд, это недорого. Но проблема в том, что цена указана не настоящая. Реальная стоимость продукта – 990 рублей. Именно такую цену вам озвучат, если вы свяжетесь с продавцами и начнете оформлять заказ. А за 147 рублей вам продадут только одну упаковку Разнотрава, лишь при условии, что две пачки порошка в купите по полной цене. Таким образом, вместе с доставкой и почтовым сбором курс лечения обойдется почти в 3 тысячи рублей.
Где купить?
Купить Разнотрав можно лишь в интернете. Продается он БАД официальном сайте. Доставка возможна только по России. Чтобы заказать продукт, нужно ввести личные данные в форму заказа. Затем кликнуть «Оформить заказ». Ожидайте – вам позвонит оператор с минуты на минуту. С ним вы обсудите все детали заказа. В случае его подтверждения на ваш адрес будет отправлена бандероль. Разнотрав заберете на почте через несколько дней.
Добро всегда накажет Зло, поставит его на колени и жестоко убьет.
-
 Андрей Эдельвейсс
Андрей Эдельвейсс
Автор темы - Трактирщик
- Сообщения: 8358
- Зарегистрирован: 29 май 2015, 19:55
- Награды: 5
- Откуда: СССР
- Род занятий: колымим
- :




- Благодарил (а): 1099 раз
- Поблагодарили: 2392 раза
- Status: Не в сети

Дневник врача частной клиники: Мы должны не вылечить пациента, а продать ему как можно больше услуг
Терапевт-гастроэнтеролог с 16-летним стажем раскрывает изнанку платной медицины
АНАСТАСИЯ ВАРДАНЯН
Терапевт-гастроэнтеролог с 16-летним стажем раскрывает изнанку платной медициныТерапевт-гастроэнтеролог с 16-летним стажем раскрывает изнанку платной медицины
Последние шесть лет Валерий работает в одном из коммерческих медцентров столицы. Его откровения мы публикуем на условиях анонимности.
«ТЫ - МЕНЕДЖЕР В БЕЛОМ ХАЛАТЕ»
- Помните, коллеги, мы живем во времена, когда деньги превыше всего. Честь, совесть, профессиональная этика - ничто. Деньги - всё! Гиппократ умер давно, а нам с вами кушать надо!
Так еженедельные совещания с нами, сотрудниками центра, начинает главврач, он же директор нашего филиала клиники. «Политику партии» у нас обсуждать не принято. Мы тут не просто врачи - менеджеры в белых халатах. С продажами все очень строго. Не выполнил план в первый раз - штраф и минимальный оклад. Не выполнил во второй раз - уволен.
В любых платных медицинских учреждениях есть план - это средний чек по пациенту. У нас это 50 тысяч рублей.
Для мотивации делают минимальный оклад и хорошую процентную ставку с каждого пациента. То есть чем больше впарил услуг, тем больше заработал.
У нас оклады от 10 до 15 тысяч рублей. Все остальное - проценты. С приема больного врач получает 20%. За направление к другому специалисту - 5%. На анализах капает 8% от потраченной пациентом суммы. У меня в месяц выходит в среднем 250 тысяч рублей. Сами понимаете, в государственной поликлинике столько никогда не заработать.
«НА ДОСКЕ ПОЧЕТА НЕ ЛУЧШИЕ ДОКТОРА, А ЛУЧШИЕ ПРОДАЖНИКИ»
Вы наверняка обращали внимание на фотографии врачей, которые во многих коммерческих центрах висят на самом видном месте у стойки ресепшен.
Это доктора, которые в этом месяце принесли в кассу больше всего денег. Как работник месяца в мебельном магазине. Смотрите, Вася Пупкин больше всех кресел продал.
Но если в продаже мебели нет ничего дурного, то у нас все наоборот. На доску почета попадают лучшие продажники. Многие болячки, из-за которых пациенты обращаются в клиники, можно вылечить после одной-двух консультаций, опираясь на симптоматику и основные общие анализы. Но так лечить совсем нерентабельно. Так вот наши передовики производства придумывают все, чтобы пациент платил, и зачастую ему, то есть пациенту, это выходит боком.
Методы надувательства у всех примерно одинаковые. Что греха таить, я ими тоже пользуюсь. Пациентов даже не надо запугивать. Когда человек пришел со своей проблемой, он уже взволнован. Достаточно просто усилить уже имеющиеся страхи всяческими намеками, покачиванием головой или парой тяжелых вздохов. Самая легкая добыча - это больные, которые в интернете начитались всяких ужасов о своих симптомах. Их мы называем «готовенькими», такие согласны на любые обследования.
Люди, поймите, нам невыгодно вас лечить. Выгодно снимать симптомы и оттягивать до последнего. Если пациент успел заработать дисбактериоз от приема бесконечного количества препаратов, это для нас просто удача. Такой больной становится совсем податливым: послушно ходит на прием и готов на все процедуры и дополнительные обследования.
В общем, действуя такими методами, только я один за двадцать рабочих дней приношу в кассу от трех миллионов рублей.
АНАЛИЗЫ - ДЕНЬГИ НА ВЕТЕР
В ситуацию, когда в коммерческом центре назначают множество анализов, попадал каждый. Поэтому о них отдельно. Во-первых, обычно нет необходимости сдавать такое количество анализов. Но вы уже прекрасно знаете про план и средний чек по каждому пациенту.
Во-вторых, вы, скорее всего, даже представить не можете, как делаются и как подделываются ваши анализы в лабораториях. Вариантов бывает несколько. Анализов вам назначили много, и вы за них заплатили баснословную сумму, но исследование в лучшем случае проводят только по самым основным или вовсе не проводят.
Почему так происходит? Скорее всего, у клиники, в которую вы пришли, плохо идут дела, поэтому она экономит. Соответственно получается недостоверная картина вашего обследования, и как следствие - неадекватное лечение. В результате здоровье не только не выправится, а, скорее всего, ухудшится. Но для медцентра это неплохо, потому что ходить сюда вы теперь будете долго и регулярно.
Второй вариант - клиники подделывают результаты. «Обнаруживают» то, чего у вас на самом деле нет. И хорошо еще, если у вас «нашли» пресловутый простатит. То есть заболевание, которое можно вылечить. Но есть клиники, которые настолько заигрались, что ставят липовые диагнозы из списка тяжелых или смертельных болезней.
И последний вариант - это клиники, которые ничего не подделывают, но благодаря грамотному менеджменту и маркетингу манипулируют пациентом, чтобы он сделал большое количество анализов и обследований. Диагноз ставят только после выполненного плана и далее назначают адекватную схему лечения.
«УГРЫЗЕНИЯ СОВЕСТИ С КАЖДЫМ ГОДОМ ВСЕ СЛАБЕЕ»
Сегодня у меня был пациент с жалобами на боль внизу живота и в паховой области. Симптомы описал следующие: неудобство при ходьбе, боли в области паха после поднятия тяжестей, чувство тяжести внизу живота. После описания симптомов возникли явные подозрения на паховую грыжу. А после осмотра и пальпации это стало очевидным.
Простая ситуация, не требующая дополнительного обследования. Можно было ему спокойно поставить диагноз и отправить к хирургу на плановую операцию. Но операции по устранению грыж в нашей клинике не проводятся, а отправить его в больницу - значит потерять клиента и получить штраф от руководства за невыполнение среднего чека по каждому пациенту.
Поэтому я его начал прогонять по нашей стандартной схеме продаж: общий анализ крови, анализы мочи, кала, УЗИ брюшной полости. Отправил к урологу в соседний кабинет. Примерная общая стоимость всех перечисленных услуг - 40 - 50 тысяч рублей.
Это мои обычные рабочие будни. Я шесть лет уже так живу, но у меня все еще бывают угрызения совести.Но с каждым годом они все слабее.
Терапевт-гастроэнтеролог с 16-летним стажем раскрывает изнанку платной медицины
АНАСТАСИЯ ВАРДАНЯН
Терапевт-гастроэнтеролог с 16-летним стажем раскрывает изнанку платной медициныТерапевт-гастроэнтеролог с 16-летним стажем раскрывает изнанку платной медицины
Последние шесть лет Валерий работает в одном из коммерческих медцентров столицы. Его откровения мы публикуем на условиях анонимности.
«ТЫ - МЕНЕДЖЕР В БЕЛОМ ХАЛАТЕ»
- Помните, коллеги, мы живем во времена, когда деньги превыше всего. Честь, совесть, профессиональная этика - ничто. Деньги - всё! Гиппократ умер давно, а нам с вами кушать надо!
Так еженедельные совещания с нами, сотрудниками центра, начинает главврач, он же директор нашего филиала клиники. «Политику партии» у нас обсуждать не принято. Мы тут не просто врачи - менеджеры в белых халатах. С продажами все очень строго. Не выполнил план в первый раз - штраф и минимальный оклад. Не выполнил во второй раз - уволен.
В любых платных медицинских учреждениях есть план - это средний чек по пациенту. У нас это 50 тысяч рублей.
Для мотивации делают минимальный оклад и хорошую процентную ставку с каждого пациента. То есть чем больше впарил услуг, тем больше заработал.
У нас оклады от 10 до 15 тысяч рублей. Все остальное - проценты. С приема больного врач получает 20%. За направление к другому специалисту - 5%. На анализах капает 8% от потраченной пациентом суммы. У меня в месяц выходит в среднем 250 тысяч рублей. Сами понимаете, в государственной поликлинике столько никогда не заработать.
«НА ДОСКЕ ПОЧЕТА НЕ ЛУЧШИЕ ДОКТОРА, А ЛУЧШИЕ ПРОДАЖНИКИ»
Вы наверняка обращали внимание на фотографии врачей, которые во многих коммерческих центрах висят на самом видном месте у стойки ресепшен.
Это доктора, которые в этом месяце принесли в кассу больше всего денег. Как работник месяца в мебельном магазине. Смотрите, Вася Пупкин больше всех кресел продал.
Но если в продаже мебели нет ничего дурного, то у нас все наоборот. На доску почета попадают лучшие продажники. Многие болячки, из-за которых пациенты обращаются в клиники, можно вылечить после одной-двух консультаций, опираясь на симптоматику и основные общие анализы. Но так лечить совсем нерентабельно. Так вот наши передовики производства придумывают все, чтобы пациент платил, и зачастую ему, то есть пациенту, это выходит боком.
Методы надувательства у всех примерно одинаковые. Что греха таить, я ими тоже пользуюсь. Пациентов даже не надо запугивать. Когда человек пришел со своей проблемой, он уже взволнован. Достаточно просто усилить уже имеющиеся страхи всяческими намеками, покачиванием головой или парой тяжелых вздохов. Самая легкая добыча - это больные, которые в интернете начитались всяких ужасов о своих симптомах. Их мы называем «готовенькими», такие согласны на любые обследования.
Люди, поймите, нам невыгодно вас лечить. Выгодно снимать симптомы и оттягивать до последнего. Если пациент успел заработать дисбактериоз от приема бесконечного количества препаратов, это для нас просто удача. Такой больной становится совсем податливым: послушно ходит на прием и готов на все процедуры и дополнительные обследования.
В общем, действуя такими методами, только я один за двадцать рабочих дней приношу в кассу от трех миллионов рублей.
АНАЛИЗЫ - ДЕНЬГИ НА ВЕТЕР
В ситуацию, когда в коммерческом центре назначают множество анализов, попадал каждый. Поэтому о них отдельно. Во-первых, обычно нет необходимости сдавать такое количество анализов. Но вы уже прекрасно знаете про план и средний чек по каждому пациенту.
Во-вторых, вы, скорее всего, даже представить не можете, как делаются и как подделываются ваши анализы в лабораториях. Вариантов бывает несколько. Анализов вам назначили много, и вы за них заплатили баснословную сумму, но исследование в лучшем случае проводят только по самым основным или вовсе не проводят.
Почему так происходит? Скорее всего, у клиники, в которую вы пришли, плохо идут дела, поэтому она экономит. Соответственно получается недостоверная картина вашего обследования, и как следствие - неадекватное лечение. В результате здоровье не только не выправится, а, скорее всего, ухудшится. Но для медцентра это неплохо, потому что ходить сюда вы теперь будете долго и регулярно.
Второй вариант - клиники подделывают результаты. «Обнаруживают» то, чего у вас на самом деле нет. И хорошо еще, если у вас «нашли» пресловутый простатит. То есть заболевание, которое можно вылечить. Но есть клиники, которые настолько заигрались, что ставят липовые диагнозы из списка тяжелых или смертельных болезней.
И последний вариант - это клиники, которые ничего не подделывают, но благодаря грамотному менеджменту и маркетингу манипулируют пациентом, чтобы он сделал большое количество анализов и обследований. Диагноз ставят только после выполненного плана и далее назначают адекватную схему лечения.
«УГРЫЗЕНИЯ СОВЕСТИ С КАЖДЫМ ГОДОМ ВСЕ СЛАБЕЕ»
Сегодня у меня был пациент с жалобами на боль внизу живота и в паховой области. Симптомы описал следующие: неудобство при ходьбе, боли в области паха после поднятия тяжестей, чувство тяжести внизу живота. После описания симптомов возникли явные подозрения на паховую грыжу. А после осмотра и пальпации это стало очевидным.
Простая ситуация, не требующая дополнительного обследования. Можно было ему спокойно поставить диагноз и отправить к хирургу на плановую операцию. Но операции по устранению грыж в нашей клинике не проводятся, а отправить его в больницу - значит потерять клиента и получить штраф от руководства за невыполнение среднего чека по каждому пациенту.
Поэтому я его начал прогонять по нашей стандартной схеме продаж: общий анализ крови, анализы мочи, кала, УЗИ брюшной полости. Отправил к урологу в соседний кабинет. Примерная общая стоимость всех перечисленных услуг - 40 - 50 тысяч рублей.
Это мои обычные рабочие будни. Я шесть лет уже так живу, но у меня все еще бывают угрызения совести.Но с каждым годом они все слабее.
Добро всегда накажет Зло, поставит его на колени и жестоко убьет.
-
 Андрей Эдельвейсс
Андрей Эдельвейсс
Автор темы - Трактирщик
- Сообщения: 8358
- Зарегистрирован: 29 май 2015, 19:55
- Награды: 5
- Откуда: СССР
- Род занятий: колымим
- :




- Благодарил (а): 1099 раз
- Поблагодарили: 2392 раза
- Status: Не в сети

Про индийские и китайские дженерики: пересказ журналистского расследования
10.06.2019 | FDA, GMP-инспекция, дженерики, контроль качества лекарственных средств 012135
Послесловие
История с индийскими и китайскими производителями не стала для меня открытием, скорее, послужила подтверждением (довольно детальным и с яркими примерами) того, что я (как и многие другие) давно подозревал. Однако мое мнение об FDA как эталоне обеспечения качества и регулирования лекарств сильно пошатнулось. Вместе с тем отмечу, что с научной и инспекционной точки зрения агентство (пока) все равно является мощнейшим; политика вносит свои уродливые коррективы в принятие решений. Европа же на этом фоне выглядит довольно порядочно, хотя без подобных расследований сложно говорить, какова внутренняя кухня. Вместе с тем подозреваю, что европейцы честнее, потому что это союз 28 (пока что) государств, поэтому скрыть нарушения гораздо сложнее. Более того, их можно признать ведущими в области обеспечения прозрачности.
Возвращаясь к нам: теперь требование о повторении исследований биоэквивалентности в России не кажется столь уж вредным, равно как и требование, чтобы наш инспекторат выезжал на зарубежные производства. Безусловно, хорошо бы наладить взаимодействие с ЕС и США по этой линии, но также важно повышение уровня наших инспекторов, обучение их навыкам сыска. Вместе с тем здесь важна рьяность и по отношению к собственным производителям. На фоне этой истории вообще можно попробовать поднять отечественную генериковую отрасль, если нацелить ее на экспорт в ЕС и США: как минимум у нас нет обезьян, а зимой еще и мух.
Фармацевтические разработка, изыскания и производство — сложные наукоемкие технологические процессы, требующие больших интеллектуальных вложений (иначе и быть не может, поскольку мы вмешиваемся в сложные процессы человеческой биохимии и генетики), поэтому невозможно одновременно достичь высокого качества, дешевизны и честности.
Что касается задач (государственного) контроля: подозрение в случае ряда компаний и стран должны трактоваться против них, то есть в пользу наших пациентов!
Это, подобное и другое про лекарства на Телеграм-канале Мета-Ф.
P.S. Спасибо Vasiliy Vlassov, что порекомендовал прочесть.
10.06.2019 | FDA, GMP-инспекция, дженерики, контроль качества лекарственных средств 012135
В середине мая 2019 г. Katherine Eban, известная своими журналистскими расследованиями, издала книгу «The Bottle of Lies» («Бутылёк лжи»), в которой обобщила результаты своего многолетнего расследования качества воспроизведенных лекарственных препаратов (генериков), производимых за рубежом для продажи на американском рынке. Ниже представлен обзор книги K. Eban «The Bottle of Lies» Равиля Ниязова (кандидат медицинских наук, специалист по разработке и регулированию лекарств, ООО «Центр научного консультирования», консультант по рынкам государств — членов Евразийского экономического союза в Корейском институте развития медицинской промышленности при Министерстве здравоохранения Южной Кореи).
В книге подробно и понятно объясняются вопросы надлежащих производственных практик (т. н. GMP), тонкости изучения, разработки и организации производства генериков, поддержания их достаточного качества и стабильности, чтобы они были столь же эффективны и безопасны, сколь оригинальные лекарства, для удешевления которых и создаются генерики.
Произведение служит хорошим примером того, как хорошее с точки зрения здоровья населения начинание в виде удешевления лекарств за счет создания более дешевых копий может быть полностью дискредитировано недобросовестной работой отдельных производителей и даже целых стран. В итоге генерики — лекарства, не отличающиеся по своему клиническому результату от оригинальных эталонов, коль скоро они разработаны и производятся в соответствии с современными научными стандартами, — понесли гигантский репутационный урон, поскольку любое благое намерение можно довести до его противоположности, если сосредоточиться исключительно на наживе, не оглядываясь на здоровье и благополучие потребителей — наиболее уязвимых категорий людей, нуждающихся в дешевых лекарствах. Но по порядку.
Книга сосредоточена на событиях с 2003 по 2017 гг., однако в ней обсуждаются как предпосылки обострения проблемы дешевых версий дорогих лекарств, так и некоторые важные события, произошедшие в 2018 г. (включая обнаружение канцерогенных примесей в антигипертензивных лекарствах — сартанах).
Проблема доступности медицинских услуг и лекарств существовала всегда, однако она сильно обострилась в середине 1980-х, когда мир внезапно поразил ВИЧ/СПИД. Особенно страдали страны Субэкваториальной Африки, в которых стремительно росло как число заболевших, так и умирающих. Появлялись первые антиретровирусные лекарства, однако их цена была столь высока, что бюджеты этих стран могли обеспечить лечение от силы нескольких тысяч человек из многомиллионной пораженной популяции с ежегодной смертностью, исчисляющейся сотнями тысяч человек. Стоимость годового курса для многих была действительно запредельной и могла доходить до 10 000 долл. США на пациента, поэтому требовалось не просто снижение цен, нужен был кардинальный обвал на несколько порядков. Однако инновационные компании довольно жестко отстаивали свои интересы, пресекая любые попытки преждевременного снятия патентной защиты, например через механизмы Всемирной торговой организации, которая защищала оригинаторов.
Но все же проблема стояла столь остро, что под давлением активных групп населения разных стран (в первую очередь США и стран Западной Европы), заручившихся поддержкой правительств большого числа государств, компании-инноваторы, желавшие избежать такого нежелательного пиара, уступили. Тогда же воодушевленные принципами Ганди индийские фармацевтические разработчики и производители заявили во всеуслышание, что Индия способна создавать дешевые лекарства и обеспечивать ими не только самые нуждающиеся развивающиеся страны, но и пациентов из государств с наиболее строгим регулированием доступа на рынок. Одним из рупоров индийского пути решения проблемы дорогих лекарств был ученый Юсуф Хамид, работавший в индийской Ципле. Это был профессионал высокого класса в области биофармацевтики и воспроизведения оригинальных лекарств. Он был идейным вдохновителем многих индийских компаний.
В США, значительно более благополучной стране, власти также испытывали колоссальное давление по созданию механизмов упрощенного доступа на рынок дешевых копий дорогих лекарств. В результате в 1984 г. году была принята поправка Хэтча-Ваксмана, давшая зеленый свет упрощенной регистрации генериков. Администрация Билла Клинтона, пришедшего к власти в 1992 г., приняла дополнительные меры по ускорению регистрации генериков (принят Закон GDUFA, который поддерживает производителей генериков), включая реорганизацию американского регулятора — FDA.
Сама история начинается с того, что американец индийского происхождения Динеш Такур, работавший в отделе по фармацевтической разработке американского фармацевтического гиганта Мерк, разрабатывающего оригинальные лекарства, в 2003 г. был приглашен индийской Ранбакси работать на историческую родину, чтобы показать всем, что Индия — это эталон современных технологий и этичного ведения бизнеса. В то время на волне обещаний индийских политиков и представителей фармацевтической отрасли дать миру дешевые генерики компания, подобно остальным, активно расширялась, чтобы удовлетворить огромный общемировой спрос на дешевые генерики. Ранбакси стала разрабатывать и производить сотни разных лекарств для большого числа стран, но наиболее лакомым рынком был американский, где можно было зарабатывать миллиарды долларов даже на генериках.
В процессе работы Динеш Такур сталкивался с различными сложностями и несоответствием фактических практик разработки, производства и документирования работы тому, чему он учился и как было заведено в Мерк. Подозрения возникали и у других недавно нанятых именитых и опытных индусов, прибывших из-за рубежа, чтобы помочь воплощать индийскую мечту. Непосредственный начальник Динеша Такура, пригласивший его на работу, уволился в течение года из-за несогласия с методами работы в компании, причем нелестно отзываясь о ней в последние дни работы. Вместо него пришел новый уважаемый и порядочный человек — Раджиндер Кумар.
Видя, что в компании есть проблемы и реагируя на первые сигналы, поступившие из Всемирной организации здравоохранения, которая поставила под сомнение качество некоторых препаратов компании, реализуемых в Африке, Такур и Кумар провели внутренний аудит и составили отчет по результатам внутренней проверки (т. н. self-assessment report, SAR, который потом руководство Ранбакси всячески пыталось скрыть от всех, но который через Такура сначала попал к FDA, а потом стал достоянием общественности), в котором говорилось, что 50–60 % лекарств, производимых компанией и отправляемых ей на американский и европейский рынки, не соответствовали заявленному качеству, а данные о биоэквивалентности были подделаны. В случае лекарств, экспортируемых на развивающиеся рынки (Африка, Ближний Восток, Юго-Восточная Азия, Южная Америка, сама Индия, Восточная Европа и Средняя Азия), отчет о внутреннем аудите указывал на почти 100%-ное несоответствие.
Такур и Кумар предложили правлению компании начать принимать соответствующие меры, чтобы разрешить сложившуюся ситуацию, но получили отказ, поскольку это подразумевало большие экономические вливания. На совещании правления на довод о том, что в Африке гибнут люди, Кумар получил ответ, что «это всего лишь черные». Не согласные, Кумар и Такур поочередно покинули Ранбакси.
Однако Такуру не давали покоя столь вопиющие нарушения, которые могли стоить большому числу людей жизни и здоровья, поэтому он принял решение анонимно проинформировать FDA о творящемся в компании. На первое письмо, которое Динеш Такур написал осенью 2005 г., ему никто не ответил, также как на второе и третье. Лишь после неоднократных обращений, в которых он все больше и больше описывал происходящее в компании, он получил первый ответ от руководства FDA, которое, однако, не спешило верить Такуру, подозревая обычный трудовой конфликт, и просило предоставить еще больше сведений. Такур писал с анонимного адреса и боялся раскрыть личность, в первую очередь опасаясь за свою безопасность и безопасность своей семьи, поскольку в Индии не действуют законы о защите информаторов, существующие в США, и поскольку семья Сингх, владевшая Ранбакси, была известна своими методами сведения счетов с неудобными людьми.
Тем не менее ему приходилось выдавать все больше и больше информации, в итоге он был вынужден передать FDA разгромный отчет о внутреннем аудите (SAR).
В своих письмах, а позже в ходе личных встреч с FDA Динеш Такур описывал, что Ранбакси подделывала данные о стабильности; без согласований переделывала формуляции, находящиеся на рынке, чтобы те лучше вели себя в испытании на растворение; подделывала отчеты об анализе на примеси, которые зашкаливали; не докладывала в препараты активные ингредиенты; на ряд препаратов вообще не вела никакие данные ни о производстве, ни о контроле. В компании была налажена схема масштабной закупки оригинальных препаратов за рубежом и завоза их на заводы Ранбакси для подделывания результатов испытаний на растворение, данных о стабильности и исследований биоэквивалентности; такой серый ввоз был практически обязанностью тех, кто выезжал в США или Европу (однажды индийский таможенник конфисковал у одного из начальников Ранбакси несколько тысяч упаковок разных лекарств, которые тот, якобы, ввозил для личных нужд). Более того, любые проверяемые во время инспектирования данные могли были быть сфабрикованы в считанные часы–дни перед инспекцией и даже во время нее.
Бюрократическая машина FDA двигалась очень медленно: только спустя 2 года после обращения агентством было принято решение устроить внеочередную проверку компании. До этого инспектированием в Индии занимался Мурал Гавини, этнический индус, который очень благосклонно относился к подконтрольным производителям, порой позволяя себе недопустимые методы работы, включая предварительное согласование инспекционного отчета с проверяемой компанией и снятие замечаний с производственной площадки во время телефонного разговора с представителем производителя. Мурал Гавини мыслил себя в качестве помощника отрасли, ее учителя, который наставлял компании, как правильно работать.
В этот раз FDA решила отправить других инспекторов для проверки одного из индийских заводов компании.
Здесь следует отметить недостаток инспекционных ресурсов в агентстве. Так, инспекции некоторых зарубежных производителей проводились не чаще чем раз в 10 лет. Кроме того, в отличие от собственных производителей, во избежание дипломатических недоразумений FDA заблаговременно уведомляло зарубежные компании о предстоящей инспекции, что, по мнению некоторых служащих агентства, являлось приглашением к непослушанию. В самих США инспекторы FDA просто приходят к любому производителю лекарства или в заведение общепита либо фермеру без предварительного уведомления (в агентстве особо никто не пользовался процедурами уведомления о предстоящей инспекции, и они даже не были проработаны). Некоторые инспекторы делают это ночью, поскольку именно тогда выявляются наиболее тяжкие злодеяния. Например, так был выявлен ресторан, подававший посетителям собачатину, а также производитель лекарств, сжигавший бракованные препараты в лесу.
Первые инспекции не выявили ничего столь серьезного, что позволило бы закрыть завод, но инспекторов не покидало ощущение, что их обманывают. Например, на одном из заводов были обнаружены две большие холодильные установки. В одной — ожидаемо — хранились лекарства для исследований. В другой хранились немаркированные лекарства для неизвестных целей. Содержимое второго холодильника в Ранбакси особо не объясняли, аргументируя тем, что это не запрещено правилами GMP.
На любые несоответствия у компании находилась тысяча объяснений и отговорок, почему что-то не соответствует положенному. У служащих FDA даже складывалось впечатление, что единственное, что хорошо получается у компании, — это оправдываться в несоответствиях. Меж тем пусть и медленно, но расследование шло своим чередом. К 2010 г. стало понятно, что масштаб нарушений превышает наихудшие предположения регулятора: работники агентства всегда считали, что компании в целом работают по правилам, только иногда допуская нарушения различной тяжести. Они и предположить не могли, что вся компания будет работать исключительно с целью создания видимости надлежащего производства и контроля и подделки регистрационной документации для доступа на мировые рынки.
Так, в конце концов выяснилось, что во втором холодильнике лежали лекарства для подделывания данных о стабильности. Стабильность оценивается в определенных условиях, например при температуре 25 градусов и влажности 60 % в течение нескольких лет. За это время происходит постепенное разложение лекарственного препарата с образованием примесей (иногда небезопасных) и снижением активности. Если разложение происходит быстрее некоторой нормы, препарат признается нестабильным. Это может объясняться, к примеру, либо неправильной разработкой препарата (например, неудачным выбором вспомогательных веществ), либо погрешностями в производстве, либо и тем и другим. В любом случае при обнаружении нестабильности препарат не должен выводиться на рынок. Холодильник же предназначался для намеренного замедления разложения лекарств за счет хранения их в прохладных условиях, в которых реакции деградации протекали гораздо медленнее, что позволяло фабрикровать данные о стабильности за счет тестирования препаратов, хранившихся в более мягких условиях деградации, и выдавая их за результаты испытаний в требуемых условиях.
В такой ситуации требовалось не просто останавливать импорт с виновных заводов (основным индийским заводам Ранбакси к тому времени уже было запрещено экспортировать лекарства в США), требовался контроль всех лекарств компании, а это чрезвычайно ресурсоемко даже для такого гиганта, как FDA. К тому же любые официальные процедуры против производителей мгновенно обрастали бюрократией, созданной во многом самим агентством для упорядочивания процессов. Требовалось «ядерное оружие», которое бы позволило скинуть с агентства бремя доказывания низкого качества лекарств и обязать производителя доказывать, что всего его лекарства, находящиеся на рынке США, качественные. И такое оружие в распоряжении FDA имелось…
Процедура Application Integrity Policy (политика безупречности досье, AIP) предусматривает приостановку регистрации всех лекарств компании, остановку импорта и налагает на производителя обязанность провести скрупулезные аудиты производства и разработки, прибегнув к услугам международных авторитетных консультантов и аудиторов, заключения которых вправе рассматривать агентство. После получения положительного заключения таких аудиторов компания обязана в индивидуальном порядке доказать, что каждый из зарегистрированных в США препаратов достоин находиться на рынке страны. Фактически процедура предполагает повторную регистрацию всех препаратов компании.
Тогда же FDA вместе с департаментом юстиции, который подключился к делу, сошлись во мнении, что на компанию нужно будет наложить большой штраф. Поначалу озвучивалась сумма, равная 3,5 млрд. долл.
Следует, однако, отметить, что расследование дела шло не так быстро, как того хотели Динеш Такур и ряд служащих FDA, которые непосредственно вели дело и видели масштаб проблем. Они недоумевали, почему Ранбакси до сих пор продает лекарства на рынке США. Очевидно, что на тот момент всё агентство знало о происходящем, однако некоторые служащие намеренно тормозили дело и не давали ему ход. Примечательно, что примерно в это же время, когда рынок США захлестнул поток лекарств из Индии, от отдельных пациентов, медицинских работников, ассоциаций клиницистов и пациентских организаций стали поступать жалобы на качество лекарств.
В 2010 г., когда FDA наконец-то запустила процедуру AIPв отношении Ранбакси, агентство получало десятки тысяч рекламаций от пациентов и врачей о некачественных генериках. В то же время другая индийская компания — «Доктор Реддис Лабораторис» (Dr. Reddy’s Laboratories) провела несколько масштабных изъятий / отзывов с рынка своего такролимуса. Такролимус — лекарство для профилактики отторжения трансплантата, имеет узкий терапевтический диапазон, поэтому высоко критично, чтобы препарат очень точно дозировался. На фоне применения препарата, которым некоторые аптеки автоматически заменяли оригинальный такролимус Програф (на основании правил замены, описанных в т. н. Оранжевой книге), отмечались случаи ухудшения состояния пациентов из-за начинающейся болезни «трансплантат против хозяина». Документированы случаи полного отторжения трансплантата. По всей стране врачи стали отговаривать пациентов принимать индийские генерики.
По признанию некоторых клиницистов после неоднократных подобных ситуаций по всей стране, они начали обращать внимание, какой производитель указан на этикетке. В книге упоминаются, в частности, случаи, когда воспроизведенный метопролол с пролонгированным высвобождением не снижал частоту сердечных сокращений, генерик торасемида не уменьшал отеки у пациентов с гипертрофической кардиомиопатией, воспроизведенный правастатин не снижал содержание холестерина в крови, пероральные сахароснижающие препараты не уменьшали гипергликемию, амлодипин не снижал артериальное давление и многое другое. Помимо упомянутых Ранбакси и Реддис, в выпуске на рынок некачественных препаратов были уличены и другие индийские компании, в том числе Ауробиндо, Гленмарк, Торрент и др.
Однако проблемы с генериками были не только у индийских компаний. Примечательна ситуация с воспроизведенным бупропионом с пролонгированным высвобождением производства израильской Тевы, которая вывела его на рынок в 2005 г.
Бупропион — это антидепрессант, разработанный компанией Valeant. Нужное терапевтическое действие бупропиона достигается при модификации его высвобождения, в том числе для сглаживания пиков концентрации. Тева вывела на американский рынок две дозировки: 150 и 300 мг. С тех пор от пациентов стали поступать различные жалобы, начиная от «невинного» плохого запаха, до тяжелых: усиления депрессии, судорог и самого грозного осложнения депрессии — суицида. Многократные обращения медицинских работников в FDA делу не помогали (говорить о том, что Тева отвергала все обвинения, излишне). Вместе с тем все же агентство запустило расследование и сообщило обращающимся, что в исследованиях биоэквивалентности изучена только меньшая дозировка (150 мг, а не 300) и что агентство считает препараты сопоставимыми, хотя налицо была клиническая несопоставимость.
Весь пересмотр данных агентство провело за «закрытыми дверями», не вынося вопрос на публичное обсуждение, причем само расследование рекламаций на качество и безопасность состояло в перепроверке старых отчетов об исследованиях биоэквивалентности без дополнительных испытаний на растворение. Однако ситуация была столь критичной, что через несколько лет FDA была вынуждена провести спонсируемое им исследование биоэквивалентности для дозировки 300 мг, в котором выяснилось, что время достижения максимальной концентрации на фоне оригинального бупропиона (Веллбутрин) —5 часов, тогда как на фоне «генерика» Тевы — 2 часа. Такой профиль высвобождения (называемый «сбросом дозы») очень хорошо объяснял клиническую картину у многих пациентов. После получения этих данных Тева отозвала свой препарат с рынка, а высокопоставленный служащий FDA, контролировавший и затягивавший все расследование, уволился из агентства и стал регуляторным директором Тевы.
Это дело, как и все дело Ранбакси, а также другие подобные, но менее известные разбирательства показали, что FDA — закрытая контора, которая не будет давать информацию и проводить расследование, если это угрожает ее корпоративным интересам.
В то же время внезапно участились случаи смерти пациентов, получавших свиной гепарин. Число жертв исчислялось десятками, а несмертельных серьезных нежелательных реакций было и того больше. Началось расследование в Конгрессе. Длительные разбирательства позволили установить причину — ряд препаратов гепарина содержали примеси гиперсульфатированного хондроитинсульфата (ГСХС), который приводил к чрезмерной антикоагулянтной активности препарата и повышению частоты жизнеугрожающих кровотечений. Один человек в этой ситуации потерял свою семью: жену и сына, которые пали жертвами такого некачественного гепарина.
Разбирательства сначала привели FDA к китайским производителям и позволили вскрыть причину: для повышения выхода гепарина, получаемого из слизистой оболочки свиней, к нему прибавляли гепаринсодержащее сырье из крупного рогатого скота — источник токсичного контаминанта. С тех пор контроль качества гепаринов в числе прочего предполагает скрининг на ГСХС. Интересно отметить, что установить виновную производственную площадку удалось не сразу, поскольку инспекторы сначала проверили не тот завод: система адресов в Китае запутана для неискушенных иностранцев, а китайские власти инспекторам FDA поддержку не оказывали. Более того, многие китайские заводы, производящие лекарственные вещества и другие фармацевтические ингредиенты на экспорт, работают в Китае в качестве химических (а не фармацевтических) производств, и поэтому подвергаются гораздо менее строгим проверкам.
Параллельно с этими событиями многолетняя бюрократическая машина FDA в 2010 г. довела дело до судебного разбирательства, то есть спустя около 5 лет после того, как Динеш Такур впервые написал в агентство о злодеяниях компании. И даже тогда все шло ни шатко ни валко. «Почему же FDA так старается предотвратить крах зарубежной индийской компании, у которой вообще нет достоверных данных?» — задавались вопросом прокуроры, сопровождавшие дело со стороны Департамента юстиции. Однако поступавшие все новые и новые порции данных двигали расследование и оформление дела вперед.
По результатам инспекций, свидетельствам многочисленных информаторов, которых данный процесс воодушевил, выяснилось, что Ранбакси для проведения исследований биоэквивалентности, испытаний на стабильность, испытаний на растворение и других тестов на качество, вкладывала в капсулы раскрошенные оригинальные препараты. Компания с легкостью подделывала хроматограммы. Ее работники срисовывали тесты на растворение, доступные в открытых источниках. Так, одна из бывших работниц Ранбакси, отвечавшая за фармаконадзор и пришедшая в компанию из Илай Лили (Eli Lilly), делилась, как она была восхищена искусности Ранбакси в разработке, когда увидела полное совпадение профилей растворения одного из препаратов компании с растворением оригинального препарата. После того как ей попался идентичный профиль растворения на другой препарат у нее стали появлятся подозрения; на третьем, четвертом и пятом препаратах она поняла, куда она попала, поэтому быстро покинула Ранбакси.
Ранбакси не гнушалась запугивать людей и даже угрожало прямыми физическими расправами тем, кто ей мешает.
На переговорах Ранбакси говорила, что «хитрить» — это культура Индии. В этой стране людям тяжело живется, поэтому приходится придумывать различные ухищрения для обхода законов. При этом административные барьеры в стране столь сложные и бессмысленные, что никто не утруждает себя их исполнением, все «хитрят» и «крутятся, как могут». Для служащих FDA же было очевидно, что культура вранья, сложившаяся в этой стране, вынуждает их сомневаться в качестве всех поступающих оттуда препаратов.
Одной из причин, почему FDA не спешила расправиться с Ранбакси (помимо внутрикорпоративных интересов и тесных связей некоторых служащих с отраслью), было сильное давление, которое испытывало агентство со стороны вышестоящих властей (Конгресса и Белого дома) и общественности по обеспечению доступности дешевых генериков, поскольку в США лекарственная помощь стоит бюджетам и обществу баснословных денег.
В частности, примерно в это же время заканчивалась патентная защита на оригинальный аторвастатин — «супер блокбастер» от Пфайзер для снижения холестерина в крови, который ежегодно приносил компании несколько миллиардов долларов. Ранбакси в свое время удалось раньше других подать заявление на регистрацию, чем она заслужила право продавать его в течение 180-дней без какой-либо конкуренции со стороны других генериков — очень заманчивая цель для любой компании, поскольку одни только продажи воспроизведенного аторвастатина сулили Ранбакси доходы, исчислявшиеся сотнями миллионов долларов.
В результате FDA, чтобы позволить Ранбакси заработать денег для выплаты штрафа, решила одобрить досье компании и выдать разрешение на продажу. Однако агентство обязало производить препарат на заводе, располагавшемся в США, в штате Нью-Джерси, который находился «под колпаком». Через неделю после того, как Ранбакси получила разрешение, она направила в FDA заявление о внесении изменений в регистрационное досье с целью переноса производственной площадки из Нью-Джерси в Индию. По административным причинам и под сильным нажимом Конгресса и общества, которые не знали о тяжелых взаимоотношениях агентства с Ранбакси (и состоянии производства лекарств в Индии в целом) FDA согласовала перенос производства — компания заработала деньги на штраф.
В 2012 г. состоялся суд, по результатам которого Ранбакси выплатила 500 млн. долл., из которых 46 млн. долл. отошли Динешу Такуру, полагавшиеся ему на основании Закона о мошенничестве (False Claims Act). Другим крупным [96 млн. долл.] получателем выплат на основании этого закона в области фармацевтики является Шерил Экард (Cheryl Eckard), раскрывшая недобросовестные производственные практики GlaxoSmithKline, которые имели место на заводе компании в Пуэрто-Рико, работавшем без обеспечения стерильности, с сильной контаминацией лекарств и т. д.
Дело Ранбакси велось за закрытыми дверями, поэтому о проблемах знали только в FDA и самой компании. Внешне Ранбакси казалась крупной успешной компанией, спасителем здравоохранения, образцом гуманизма, но умеющей вести бизнес. Примерно в 2008–2009 гг. ею заинтересовалась японская Дайичи Санкьё, а в 2010 г. приобрела контрольный пакет. Никакие аудиты не позволили руководству Дайичи Санкьё узнать истинные нарушения Ранбакси и те проблемы, из-за которых ее прессовала FDA. Отчет о внутреннем аудите (SAR) стал доступен инвестору, вложившему в индийского гиганта 2 млрд. долл., только после суда в США, когда Дайичи Санкьё узнала истинное положение вещей. И даже после этого Малвиндер Сингх все отрицал.
Вся эта история привела FDA к осознанию, что проведение инспекций зарубежных производителей в уведомительном порядке является напрасной тратой ресурсов, поэтому она вела переговоры с индийскими властями о создании в стране собственного офиса для инспектирования. И такое разрешение она получила. Одним из первых инспекторов индийского офиса стал Питер Бейкер (посмотрите его профиль на LindedIn). Бейкер был одаренным инспектором, можно сказать сыщиком: он умел находить то, что пропустили другие. У него было чутье на нарушения: даже легкие на первый взгляд «странности», на которые бы другой не обратил внимание, нередко приводили к вскрытию им колоссальных нарушений.
В частности, инспекция Бейкером завода компании Вокхарт в 2013 г. показала, что данные на инсулин отсутствуют или не соответствуют фактически производимому препарату. В частности, он обнаружил секретные линии производства с черными металлическими (!) включениями. Препарат не продается в США, как отмечает автор, но до сих пор на рынке других стран (арабские страны, страны Африки, Россия) [от себя: это тот же самый инсулин, в регистрации которого в том же 2013 г. отказало Европейское агентство по лекарствам, поскольку данные о его разработке не соответствовали препарату, который производится компанией в настоящее время: отсутствовали данные о валидации производства препарата, который бы соответствовал препарату, изученному в опорных клинических исследованиях (т. н. в глюкозных клэмпах); для наших экспертов по качеству это не явилось препятствием].
В другом случае Бейкер наткнулся на неправильно укупоренный и тем самым нестерильный гемцитабин — противоопухолевое средство для парентерального введения; препарат шел на американский рынок.
Что характерно, масштабные нарушения со стороны индийских компаний продолжались и после того, как Ранбакси была оштрафована на огромную сумму. В ходе своего пребывания в Индии Бейкер столкнулся с уничтожением данных прямо на его глазах, бегством работников, пойманных с документальным подтверждением нарушений, мочой в производственных зонах, обнаружением гнездовий птиц, змей, нашествием обезьян на производственные площадки, полчищами мух в стерильных производствах; секретными формуляционными линиями. и т. д. Бейкера удивляло, что заводы располагали достаточными техническими и инфраструктурными возможностями, но тратили их на подделку как самих лекарств, так и документации.
По этой причине производители делали все возможное, чтобы заранее выяснить, куда будут направляться инспекторы, а также принимали меры для воспрепятствования ходу инспекции. В частности, были случаи, когда инспекторам подмешивали снотворное, в ответ перед посещением площадки инспекторы стали продумывать план экстренной эвакуации. Были случаи, когда для отправки инспекционных находок в головной офис FDA по вызову инспекторов приезжали подставные работники DHL. Были случаи, когда инспекторы обнаруживали, что их номера в отелях прослушиваются, в результате инспектируемые лица были готовы к заранее продуманному плану инспектирования. Работники индийского офиса FDA также допускали утечку информации, поэтому инспекторы вообще перестали их информировать, а потом и отказались от идеи индийского офиса. Были неоднократные попытки подкупа, вероятно, где-то успешные: несмотря на отсутствие прямых доказательств агентство сильно подозревало инспектора Мурала Гавини, этнического индуса, в сговоре с индийскими производителями. Как ни странно, FDA было очень тяжело избавиться от него.
Инспекторы стали прилетать на инспекции по дипломатическим каналам, возложив все мероприятия по организации инспекций на сотрудников государственного департамента США. В итоге компании стали вести мониторинг аэропортов и отелей для отслеживания прибытия инспекторов.
Однажды Бейкер с напарником прибыли на инспекцию, о проведении которой сообщили за несколько дней до ее начала. Первым днем инспекции должен был быть понедельник, однако приехали они туда в воскресенье, никому заранее не сообщив об этом. Завод был полон работников, которые дружно уничтожали документацию, мыли помещения и другим образом заметали следы. Окна в стерильных производственных зонах были открыты настежь, везде летали мухи, люди ходили босиком. Инспекторов распознали не сразу — увидев двух людей европейской внешности, сотрудники завода подумали, что это очередные аудиторы, поэтому продолжали свою деятельность как ни в чем не бывало.
В другом случае Бейкер с напарником нашли лабораторию с идеальными документированными результатами, которая однако вообще ничего реально не тестировала и содержалась производителем только ради фабрикации результатов испытаний; на дворе стоял 2014 год.
Хорошим способом понять что к чему Бейкер считал разговор с рядовыми работниками, у которых можно было выудить ценнейшую информацию о нарушениях. Как-то поймав одного такого рабочего, который пытался скрыть очередную порцию документов, тот взмолился, что не может признаться, ибо боится потерять работу, которую в Индии очень тяжело найти. По этой причине приходиться идти на нарушения и на многое закрывать глаза. Бейкер понимал, что нищенские условия рабочих, высокая неграмотность, социальная и трудовая незащищенность, страх потерять работу вседозволенность для власть предержащих создавали оптимальные условия для масштабных нарушений.
В одном из интервью в 2015 г. глава индийского регулятора открыто обмолвился, что если они будут проводить инспектирование по западным стандартам, то Центральная организация по контролю стандартизации лекарств — лекарственный регулятор Индии — будет вынуждена закрыть почти все фармацевтические заводы, располагающиеся в стране.
Бейкер отмечал, что инспекторы фактически обучают индийских производителей тому, как можно нарушать и не быть пойманным; никто и не помышлял начинать производить лекарства по правилам. Почти все лекарства имели ту или иную степень брака, причем более некачественная продукция сбывалась на развивающиеся рынки. Серии, не выдержавшие испытания, на одном из индийских заводов, располагавшегося к югу от Хайдерабада и производящего препараты для американского рынка, отправлялись по признанию самого руководства завода на украинский рынок (глава 26). Альтернативные производственные линии — обычная практика. Если страна предъявляет высокие требования к качеству, то препараты выпускаются на «хорошей линии»; если требования страны к качеству лекарств низкие, то предусмотрены отдельные линии для экономии ресурсов. Худшая, бракованная и отвергнутая продукция (даже по индийским меркам) отправлялась на три основных рынка: в Экваториальную и Субэкваториальную Африку, Южную Америку и Восточную Европу. Руководство какой-то из индийской компаний так и говорило: каким бы плохим ни было «лекарство», всегда найдутся его покупатели.
Примечательна ситуация в Африке. В Уганде врачи, работавшие по линии «Врачей без границ» в 2013 г. стали отмечать, что некоторые лекарства для лечения инфекционных гнойно-септических заболеваний не помогают их пациентам. Некоторые даже подозревали возникновение новых патогенов, однако более опытные коллеги давно знали, в чем может быть дело. Стоило пациенту дать оригинальное лекарство или неиндийский генерик, как он почти наверняка шел на поправку, однако такие лекарства из-за их дороговизны держали в качестве резерва. Подобное «чудодейственное» выздоровление в Уганде прозвали «эффектом Лазаря». Основной проблемой в случае противомикробных лекарств было меньшее, чем положено, содержание активных ингредиентов, ибо это не только угрожало конкретному пациенту, но и стало одной из причин — согласно докладам ВОЗ — формирования широкой антибиотикорезистентности. Однако на ситуацию в Уганде было достаточно тяжело повлиять, поскольку препараты закупались без какого-либо контроля. Лишь в 2016–2017 гг. в стране заработала лаборатория по контролю качества лекарств, находящихся на рынке.
Многие служащие FDA признавались автору книги, что после всего обнаруженного они стали принимать все возможные меры, чтобы избегать назначения себе и своим семьям генериков из Индии, а некоторые — рубежные генерики вообще, о чем они даже заявляли публично на слушаниях в Конгрессе. На одном из заседаний, они сокрушались: «Если бы только люди вникли и осознали, какая это опасность и мошенничество, они бы не принимали генерики, производимые таким образом».
В 2015 году Бейкер покинул Индию и переехал в Китай для инспектирования производителей активных фармацевтических ингредиентов. Самая первая инспекция в Китае была на контрактной производственной площадке Пфайзер. Компания работала с китайским производителем для получения аторвастатина вот уже 3 года. Нареканий со стороны отдела обеспечения качества Пфайзер не было, поэтому доверия к китайским производителям было больше. В первый же день инспектирования Бейкер направился в аналитическую лабораторию по контролю качества. В университете он изучал китайский, поэтому попросив сотрудника лаборатории предоставить доступ к компьютеру, он стал искать иероглифы, обозначавшие «пробный анализ» и т. п. В первый же день он вскрыл систему двойного документооборота, о которой в Пфайзер даже не подозревали! Через год компания прекратила сотрудничество с заводом.
На другом из заводов Бейкер к своему удивлению обнаружил шредер посреди производственного цеха. Само по себе это не преступно, но сеет подозрения. В результате на этой производственной площадке также были обнаружены критические ошибки. На повторной инспекции шредер исчез из цеха, но обнаружился в итоге в аналитической лаборатории. Из других находок часто встречались не документируемые «пробные» испытания, незарегистрированное контрольное оборудование (хроматографы) и т. п.
До Бейкера китайские производители были крепким орешком для контролеров из Европы и Северной Америки. Сами же китайцы, по описанию автора книги, составленной ей на основании разговоров с представителями регуляторов, американскими производителями и информаторами с китайских заводов, считали чуть ли не своей обязанностью водить за нос проверяющих, приезжающих с Запада. Были случаи, когда под видом разных заводов инспекторов из разных стран возили на один и тот же. Была практика демонстрации образцовых производств и лабораторий, в реальности никогда не производивших лекарства и т. д. Ситуация была очень похожа на положение вещей в Индии.
Китайские производители, до того особо не встречавшие проблем с одурачиванием инспекторов, стали сильно боятся Бейкера. Тот же один за другим выдавал отчеты по форме 483 с заключением OAI. Форма 483 — форма отчета об инспекции FDA; OAI— official action indicated (показано принятие официальных мер) — оборот, означающий запрет заводу поставлять продукцию на рынок до устранения недочетов. Тогда как VAI — voluntary action indicated (показано принятие добровольных мер) — оборот для обозначения небольших недочетов, устраняемых без запрета выпуска на рынок. Наконец, NAI (no action indicated) — принятие мер не требуется.
Однако такое больше число OAI от Бейкера в отношении китайских заводов отнюдь не радовало высшие чины FDA, наоборот, это было проблемой. Конгресс и Администрация президента оказывали на FDA давление по обеспечению доступа к дешевым лекарствам, что предполагало увеличение числа производителей (и Китай вместе с Индией здесь занимал ведущие позиции), а не их сокращение. Многие предложения Бейкера о согласовании OAI отклонялись и снижались до VAI, что позволяло заводам дальше поставлять бракованную продукцию на рынок США.
Несмотря на то что Бейкер был героем среди рядовых инспекторов, в агентстве не все радовались его успехам и достижениям. Руководство FDA говорило, что они не могут требовать от всех своих служащих такого рвения в работе (в том числе ковыряние в мусорках), инспектирования во внеурочное время и т. д.
Вместе с тем в Евросоюзе он был очень популярен среди инспекторов: его регулярно приглашали, чтобы обучить европейцев подходам Бейкера к выявлению недобросовестности при производстве и контроле на китайских и индийских производствах (от себя: на официальном YouTube-канале EMA есть хороший видеокурс по тренингу инспекторов:
Однако несмотря на все заслуги Бейкера, корпоративные интересы FDA все же возобладали, и 2018 г. он был отозван из Китая и переведен в чилийский офис агентства. Однако там ему не давали каких-либо серьезных заданий, поэтому он покинул агентство в том же году и начал работать GMP-аудитором.
Смотря на ситуацию с зарубежными генериками, продаваемыми на американском рынке, интересно также взглянуть на генериковую отрасль самих Штатов.
Одним из основных игроков в стране и флагманом надлежащих практик в этой области была компания Mylan. Именно работники Mylan в 1988 г., то есть спустя 4 года после узаконивания сокращенного механизма одобрения генериков в США (закон Хэтча-Ваксмана), вскрыли масштабную коррупцию в офисе воспроизведенных лекарств FDA. Office of Generic Drugs, OGD — подразделение FDA, занимающееся экспертизой генериков и составляющее те самые препаратспецифичные монографии на генерики, число которых приблизилось к 1700; с точки зрения научного потенциала людям оттуда нет равных среди регуляторов. Однако в тот год несколько служащих OGD FDA были уличены в почти неприкрытых взятках в виде дорогих путешествий, подарков и т. д., которыми они вознаграждались за выдачу разрешений конкурентам Mylan’а. Например, в случае одного из экспертов FDA улики были обнаружены в мусорном ведре его дома: это были чеки на покупки, которые служащий не смог бы приобрести при его уровне заработка на госслужбе.
Предпосылки для коррупции были созданы самим агентством, по предложению которого, в рамках закона Хэтча-Ваксмана была согласована возможность предоставления 180-дневной рыночной исключительности первому зарегистрированному генерику. Это норма имела вполне логичное обоснование: вывод первого генерика может так или иначе сопровождаться нарушением патентных прав оригинатора. Тот, свою очередь, конечно же, будет защищать свои интересы в суде и может победить, в связи с чем первый разработчик может понести существенные потери. Для вознаграждения риска, на который идет первый разработчик генерика, и была введена норма о 180-дневной исключительности первого генерика.
Поскольку дата истечения патента в целом была известна (она указывается в Оранжевой книге), довольно регулярно возникали ситуации, когда на парковке перед офисом воспроизведенных лекарств FDA еще за несколько дней до предполагаемой даты возможной подачи заявления на регистрацию генерика (т. н. ANDA — сокращенное заявление на новое лекарство) собирались очереди, а в день подачи иногда даже случались потасовки между представителями разных компаний. Однако все на этом не заканчивалось, поскольку принятым считалось только существенно полное досье (substantially complete ANDA). Разумеется, полнота досье выяснялась служащими FDA позднее. Такая неразбериха и предоставление 180-дневной исключительности создавали почву для манипуляций и злоупотреблений, приведших к кризису 1988 г. Лишь 1992 г. FDA исправила положение вещей, решив предоставлять 180-дневную исключительность всем компаниям, первым подавшим ANDA в один и тот же день.
Благодаря этой истории Майлэн снискала славу этичной и честной компании, отстаивавшей принципы добросовестного ведения бизнеса. Однако в начале нового тысячелетия компания также начала испытывать конкуренцию со стороны зарубежных генериковых компаний и принимала соответствующие меры. Одной из таких мер был наем Юсуфа Хамида (см. выше) из индийской Циплы, идейного вдохновителя индийского генерического «чуда», в качестве специалиста по фармацевтической разработке для улучшения квалификации Mylan в этой сфере. Юсуф Хамид действительно принес новые знания и позволил Mylan многого добиться с точки зрения расширения продуктового портфеля. Сам он постепенно добрался до правления американской компании — нечастое явление для иностранца.
Однако столь стремительный успех дался компании не на пустом месте: вместе с собой Хамид привел свою индийскую команду разработчиков. Хамид и его команда, пусть открыто и не прибегали к индийским методам, но все же ряд сотрудников стал отмечать, что целью Хамида была регистрация максимального числа препаратов (от этого в том числе зависел его заработок), при этом высокое качество, постоянство производства и стабильность препарата стояли далеко не на первом месте, поэтому бракованная продукция перестала быть редкостью, участились отзывы продукции с рынка.
Кроме того, в правление компании вошла дочь одного из сенаторов Конгресса, что также упрочило позиции компании на политической арене, поэтому ряд проблем производства и качества стали решаться политическими мерами. Это также не пошло на пользу имиджу Mylan. В результате компания, осознав, в какой ситуации она оказалась, в 2018 г. избавилась от Хамида и его команды, равно как и от дочки сенатора и пытается теперь восстановить свою пошатнувшуюся репутацию.
Все произошедшие за это время пертурбации с генериками вынудили Кливлендскую клинику (Cleveland Clinic, штат Огайо) — одного из ведущих академических медицинских центров страны, являющегося, возможно, самым взыскательным покупателем лекарств в США, прийти к выводу, что нужно избегать определенных фармацевтических производителей. При этом простые люди должны получить возможность принимать информированные решения, основанные на знании рисковых производителей.
Сегодня Ранбакси больше нет. В 2014 г. очередной информатор, сообщил материнской компании — японской Дайичи Санкьё, что персонал Ранбакси подмешивал в активные ингредиенты дешевые некачественные загрязненные полупродукты, вел двойную документацию (настоящую и для регуляторов), отбеливал желтые из-за примесей таблетки, которые должны были быть белыми, прятал улики сначала под потолочными плитами, а потом выбрасывал в реку. Дайичи Санкьё решила избавиться от Ранбакси и продала ее индийской Сан Фармасьютикалз: бренд Ранбакси перестал существовать. (Однако если поискать «Ранбакси» в госреестре лекарственных средств, то обнаружится, что за этой несуществующей компании все еще числится ряд лекарств с действующими регистрационными удостоверениями).
Более того, Дайичи Санкьё подала в суд на самого Малвиндера Сингха в международный арбитраж в Сингапуре, отсудив у него 850 млн. долл. за недобросовестные практики. Даже Верховный суд Индии, защиты которого просил Сингх, оставил в силе постановление Сингапурского суда. Сам Сингх все отрицал до последнего и продолжает выставлять жертвой себя. (В татарском языке есть поговорка в отношении подобных людей, которую можно перевести как «давать под зад, глядя в глаза»).
Однако исчезновение Ранбакси не означает, что исчезли люди. Представителей бывшего топ-менеджмента компании, известных своими навыками создания досье ещё до завершения фармацевтической разработки, можно признать одними из лучших фальсификаторов в фармацевтической отрасли. Теперь они проникли в другие компании.
Казалось бы, что история закончилась, враг побежден. Однако в 2016 г. на весь мир прогремел запрет Евросоюзом около 700 лекарств, оценка биоэквивалентности которых проводилась в одном из клинических центров Индии: французские GCP-инспекторы вскрыли подделывание ЭКГ. На основании этого они усомнились во всех остальных данных, полученных в этом исследовательском центре. FDA какие-то меры приняла, но полностью препараты не запретила.
Уже в 2018 г. Европа вскрыла масштабную загрязненность генериковых антагонистов рецепторов ангиотензина II («сартанов») генотоксичными примесями — нитрозаминовыми производными. При этом виновная Чжэцзян Хуахай (опять же посмотрите на сартаны в нашем госреестре) признала, что процесс, приводивший к образованию таких примесей, действовал с 2012 г. Новость из Европы застала FDA врасплох, хотя не должна была: еще в 2017 г. во время инспекции было выявлено зашкаливание примесей и инспекторы FDA предлагали OAI, но функционеры агентства снизили его до VAI и забыли про дело.
В книге подробно и понятно объясняются вопросы надлежащих производственных практик (т. н. GMP), тонкости изучения, разработки и организации производства генериков, поддержания их достаточного качества и стабильности, чтобы они были столь же эффективны и безопасны, сколь оригинальные лекарства, для удешевления которых и создаются генерики.
Произведение служит хорошим примером того, как хорошее с точки зрения здоровья населения начинание в виде удешевления лекарств за счет создания более дешевых копий может быть полностью дискредитировано недобросовестной работой отдельных производителей и даже целых стран. В итоге генерики — лекарства, не отличающиеся по своему клиническому результату от оригинальных эталонов, коль скоро они разработаны и производятся в соответствии с современными научными стандартами, — понесли гигантский репутационный урон, поскольку любое благое намерение можно довести до его противоположности, если сосредоточиться исключительно на наживе, не оглядываясь на здоровье и благополучие потребителей — наиболее уязвимых категорий людей, нуждающихся в дешевых лекарствах. Но по порядку.
Книга сосредоточена на событиях с 2003 по 2017 гг., однако в ней обсуждаются как предпосылки обострения проблемы дешевых версий дорогих лекарств, так и некоторые важные события, произошедшие в 2018 г. (включая обнаружение канцерогенных примесей в антигипертензивных лекарствах — сартанах).
Проблема доступности медицинских услуг и лекарств существовала всегда, однако она сильно обострилась в середине 1980-х, когда мир внезапно поразил ВИЧ/СПИД. Особенно страдали страны Субэкваториальной Африки, в которых стремительно росло как число заболевших, так и умирающих. Появлялись первые антиретровирусные лекарства, однако их цена была столь высока, что бюджеты этих стран могли обеспечить лечение от силы нескольких тысяч человек из многомиллионной пораженной популяции с ежегодной смертностью, исчисляющейся сотнями тысяч человек. Стоимость годового курса для многих была действительно запредельной и могла доходить до 10 000 долл. США на пациента, поэтому требовалось не просто снижение цен, нужен был кардинальный обвал на несколько порядков. Однако инновационные компании довольно жестко отстаивали свои интересы, пресекая любые попытки преждевременного снятия патентной защиты, например через механизмы Всемирной торговой организации, которая защищала оригинаторов.
Но все же проблема стояла столь остро, что под давлением активных групп населения разных стран (в первую очередь США и стран Западной Европы), заручившихся поддержкой правительств большого числа государств, компании-инноваторы, желавшие избежать такого нежелательного пиара, уступили. Тогда же воодушевленные принципами Ганди индийские фармацевтические разработчики и производители заявили во всеуслышание, что Индия способна создавать дешевые лекарства и обеспечивать ими не только самые нуждающиеся развивающиеся страны, но и пациентов из государств с наиболее строгим регулированием доступа на рынок. Одним из рупоров индийского пути решения проблемы дорогих лекарств был ученый Юсуф Хамид, работавший в индийской Ципле. Это был профессионал высокого класса в области биофармацевтики и воспроизведения оригинальных лекарств. Он был идейным вдохновителем многих индийских компаний.
В США, значительно более благополучной стране, власти также испытывали колоссальное давление по созданию механизмов упрощенного доступа на рынок дешевых копий дорогих лекарств. В результате в 1984 г. году была принята поправка Хэтча-Ваксмана, давшая зеленый свет упрощенной регистрации генериков. Администрация Билла Клинтона, пришедшего к власти в 1992 г., приняла дополнительные меры по ускорению регистрации генериков (принят Закон GDUFA, который поддерживает производителей генериков), включая реорганизацию американского регулятора — FDA.
Сама история начинается с того, что американец индийского происхождения Динеш Такур, работавший в отделе по фармацевтической разработке американского фармацевтического гиганта Мерк, разрабатывающего оригинальные лекарства, в 2003 г. был приглашен индийской Ранбакси работать на историческую родину, чтобы показать всем, что Индия — это эталон современных технологий и этичного ведения бизнеса. В то время на волне обещаний индийских политиков и представителей фармацевтической отрасли дать миру дешевые генерики компания, подобно остальным, активно расширялась, чтобы удовлетворить огромный общемировой спрос на дешевые генерики. Ранбакси стала разрабатывать и производить сотни разных лекарств для большого числа стран, но наиболее лакомым рынком был американский, где можно было зарабатывать миллиарды долларов даже на генериках.
В процессе работы Динеш Такур сталкивался с различными сложностями и несоответствием фактических практик разработки, производства и документирования работы тому, чему он учился и как было заведено в Мерк. Подозрения возникали и у других недавно нанятых именитых и опытных индусов, прибывших из-за рубежа, чтобы помочь воплощать индийскую мечту. Непосредственный начальник Динеша Такура, пригласивший его на работу, уволился в течение года из-за несогласия с методами работы в компании, причем нелестно отзываясь о ней в последние дни работы. Вместо него пришел новый уважаемый и порядочный человек — Раджиндер Кумар.
Видя, что в компании есть проблемы и реагируя на первые сигналы, поступившие из Всемирной организации здравоохранения, которая поставила под сомнение качество некоторых препаратов компании, реализуемых в Африке, Такур и Кумар провели внутренний аудит и составили отчет по результатам внутренней проверки (т. н. self-assessment report, SAR, который потом руководство Ранбакси всячески пыталось скрыть от всех, но который через Такура сначала попал к FDA, а потом стал достоянием общественности), в котором говорилось, что 50–60 % лекарств, производимых компанией и отправляемых ей на американский и европейский рынки, не соответствовали заявленному качеству, а данные о биоэквивалентности были подделаны. В случае лекарств, экспортируемых на развивающиеся рынки (Африка, Ближний Восток, Юго-Восточная Азия, Южная Америка, сама Индия, Восточная Европа и Средняя Азия), отчет о внутреннем аудите указывал на почти 100%-ное несоответствие.
Такур и Кумар предложили правлению компании начать принимать соответствующие меры, чтобы разрешить сложившуюся ситуацию, но получили отказ, поскольку это подразумевало большие экономические вливания. На совещании правления на довод о том, что в Африке гибнут люди, Кумар получил ответ, что «это всего лишь черные». Не согласные, Кумар и Такур поочередно покинули Ранбакси.
Однако Такуру не давали покоя столь вопиющие нарушения, которые могли стоить большому числу людей жизни и здоровья, поэтому он принял решение анонимно проинформировать FDA о творящемся в компании. На первое письмо, которое Динеш Такур написал осенью 2005 г., ему никто не ответил, также как на второе и третье. Лишь после неоднократных обращений, в которых он все больше и больше описывал происходящее в компании, он получил первый ответ от руководства FDA, которое, однако, не спешило верить Такуру, подозревая обычный трудовой конфликт, и просило предоставить еще больше сведений. Такур писал с анонимного адреса и боялся раскрыть личность, в первую очередь опасаясь за свою безопасность и безопасность своей семьи, поскольку в Индии не действуют законы о защите информаторов, существующие в США, и поскольку семья Сингх, владевшая Ранбакси, была известна своими методами сведения счетов с неудобными людьми.
Тем не менее ему приходилось выдавать все больше и больше информации, в итоге он был вынужден передать FDA разгромный отчет о внутреннем аудите (SAR).
В своих письмах, а позже в ходе личных встреч с FDA Динеш Такур описывал, что Ранбакси подделывала данные о стабильности; без согласований переделывала формуляции, находящиеся на рынке, чтобы те лучше вели себя в испытании на растворение; подделывала отчеты об анализе на примеси, которые зашкаливали; не докладывала в препараты активные ингредиенты; на ряд препаратов вообще не вела никакие данные ни о производстве, ни о контроле. В компании была налажена схема масштабной закупки оригинальных препаратов за рубежом и завоза их на заводы Ранбакси для подделывания результатов испытаний на растворение, данных о стабильности и исследований биоэквивалентности; такой серый ввоз был практически обязанностью тех, кто выезжал в США или Европу (однажды индийский таможенник конфисковал у одного из начальников Ранбакси несколько тысяч упаковок разных лекарств, которые тот, якобы, ввозил для личных нужд). Более того, любые проверяемые во время инспектирования данные могли были быть сфабрикованы в считанные часы–дни перед инспекцией и даже во время нее.
Бюрократическая машина FDA двигалась очень медленно: только спустя 2 года после обращения агентством было принято решение устроить внеочередную проверку компании. До этого инспектированием в Индии занимался Мурал Гавини, этнический индус, который очень благосклонно относился к подконтрольным производителям, порой позволяя себе недопустимые методы работы, включая предварительное согласование инспекционного отчета с проверяемой компанией и снятие замечаний с производственной площадки во время телефонного разговора с представителем производителя. Мурал Гавини мыслил себя в качестве помощника отрасли, ее учителя, который наставлял компании, как правильно работать.
В этот раз FDA решила отправить других инспекторов для проверки одного из индийских заводов компании.
Здесь следует отметить недостаток инспекционных ресурсов в агентстве. Так, инспекции некоторых зарубежных производителей проводились не чаще чем раз в 10 лет. Кроме того, в отличие от собственных производителей, во избежание дипломатических недоразумений FDA заблаговременно уведомляло зарубежные компании о предстоящей инспекции, что, по мнению некоторых служащих агентства, являлось приглашением к непослушанию. В самих США инспекторы FDA просто приходят к любому производителю лекарства или в заведение общепита либо фермеру без предварительного уведомления (в агентстве особо никто не пользовался процедурами уведомления о предстоящей инспекции, и они даже не были проработаны). Некоторые инспекторы делают это ночью, поскольку именно тогда выявляются наиболее тяжкие злодеяния. Например, так был выявлен ресторан, подававший посетителям собачатину, а также производитель лекарств, сжигавший бракованные препараты в лесу.
Первые инспекции не выявили ничего столь серьезного, что позволило бы закрыть завод, но инспекторов не покидало ощущение, что их обманывают. Например, на одном из заводов были обнаружены две большие холодильные установки. В одной — ожидаемо — хранились лекарства для исследований. В другой хранились немаркированные лекарства для неизвестных целей. Содержимое второго холодильника в Ранбакси особо не объясняли, аргументируя тем, что это не запрещено правилами GMP.
На любые несоответствия у компании находилась тысяча объяснений и отговорок, почему что-то не соответствует положенному. У служащих FDA даже складывалось впечатление, что единственное, что хорошо получается у компании, — это оправдываться в несоответствиях. Меж тем пусть и медленно, но расследование шло своим чередом. К 2010 г. стало понятно, что масштаб нарушений превышает наихудшие предположения регулятора: работники агентства всегда считали, что компании в целом работают по правилам, только иногда допуская нарушения различной тяжести. Они и предположить не могли, что вся компания будет работать исключительно с целью создания видимости надлежащего производства и контроля и подделки регистрационной документации для доступа на мировые рынки.
Так, в конце концов выяснилось, что во втором холодильнике лежали лекарства для подделывания данных о стабильности. Стабильность оценивается в определенных условиях, например при температуре 25 градусов и влажности 60 % в течение нескольких лет. За это время происходит постепенное разложение лекарственного препарата с образованием примесей (иногда небезопасных) и снижением активности. Если разложение происходит быстрее некоторой нормы, препарат признается нестабильным. Это может объясняться, к примеру, либо неправильной разработкой препарата (например, неудачным выбором вспомогательных веществ), либо погрешностями в производстве, либо и тем и другим. В любом случае при обнаружении нестабильности препарат не должен выводиться на рынок. Холодильник же предназначался для намеренного замедления разложения лекарств за счет хранения их в прохладных условиях, в которых реакции деградации протекали гораздо медленнее, что позволяло фабрикровать данные о стабильности за счет тестирования препаратов, хранившихся в более мягких условиях деградации, и выдавая их за результаты испытаний в требуемых условиях.
В такой ситуации требовалось не просто останавливать импорт с виновных заводов (основным индийским заводам Ранбакси к тому времени уже было запрещено экспортировать лекарства в США), требовался контроль всех лекарств компании, а это чрезвычайно ресурсоемко даже для такого гиганта, как FDA. К тому же любые официальные процедуры против производителей мгновенно обрастали бюрократией, созданной во многом самим агентством для упорядочивания процессов. Требовалось «ядерное оружие», которое бы позволило скинуть с агентства бремя доказывания низкого качества лекарств и обязать производителя доказывать, что всего его лекарства, находящиеся на рынке США, качественные. И такое оружие в распоряжении FDA имелось…
Процедура Application Integrity Policy (политика безупречности досье, AIP) предусматривает приостановку регистрации всех лекарств компании, остановку импорта и налагает на производителя обязанность провести скрупулезные аудиты производства и разработки, прибегнув к услугам международных авторитетных консультантов и аудиторов, заключения которых вправе рассматривать агентство. После получения положительного заключения таких аудиторов компания обязана в индивидуальном порядке доказать, что каждый из зарегистрированных в США препаратов достоин находиться на рынке страны. Фактически процедура предполагает повторную регистрацию всех препаратов компании.
Тогда же FDA вместе с департаментом юстиции, который подключился к делу, сошлись во мнении, что на компанию нужно будет наложить большой штраф. Поначалу озвучивалась сумма, равная 3,5 млрд. долл.
Следует, однако, отметить, что расследование дела шло не так быстро, как того хотели Динеш Такур и ряд служащих FDA, которые непосредственно вели дело и видели масштаб проблем. Они недоумевали, почему Ранбакси до сих пор продает лекарства на рынке США. Очевидно, что на тот момент всё агентство знало о происходящем, однако некоторые служащие намеренно тормозили дело и не давали ему ход. Примечательно, что примерно в это же время, когда рынок США захлестнул поток лекарств из Индии, от отдельных пациентов, медицинских работников, ассоциаций клиницистов и пациентских организаций стали поступать жалобы на качество лекарств.
В 2010 г., когда FDA наконец-то запустила процедуру AIPв отношении Ранбакси, агентство получало десятки тысяч рекламаций от пациентов и врачей о некачественных генериках. В то же время другая индийская компания — «Доктор Реддис Лабораторис» (Dr. Reddy’s Laboratories) провела несколько масштабных изъятий / отзывов с рынка своего такролимуса. Такролимус — лекарство для профилактики отторжения трансплантата, имеет узкий терапевтический диапазон, поэтому высоко критично, чтобы препарат очень точно дозировался. На фоне применения препарата, которым некоторые аптеки автоматически заменяли оригинальный такролимус Програф (на основании правил замены, описанных в т. н. Оранжевой книге), отмечались случаи ухудшения состояния пациентов из-за начинающейся болезни «трансплантат против хозяина». Документированы случаи полного отторжения трансплантата. По всей стране врачи стали отговаривать пациентов принимать индийские генерики.
По признанию некоторых клиницистов после неоднократных подобных ситуаций по всей стране, они начали обращать внимание, какой производитель указан на этикетке. В книге упоминаются, в частности, случаи, когда воспроизведенный метопролол с пролонгированным высвобождением не снижал частоту сердечных сокращений, генерик торасемида не уменьшал отеки у пациентов с гипертрофической кардиомиопатией, воспроизведенный правастатин не снижал содержание холестерина в крови, пероральные сахароснижающие препараты не уменьшали гипергликемию, амлодипин не снижал артериальное давление и многое другое. Помимо упомянутых Ранбакси и Реддис, в выпуске на рынок некачественных препаратов были уличены и другие индийские компании, в том числе Ауробиндо, Гленмарк, Торрент и др.
Однако проблемы с генериками были не только у индийских компаний. Примечательна ситуация с воспроизведенным бупропионом с пролонгированным высвобождением производства израильской Тевы, которая вывела его на рынок в 2005 г.
Бупропион — это антидепрессант, разработанный компанией Valeant. Нужное терапевтическое действие бупропиона достигается при модификации его высвобождения, в том числе для сглаживания пиков концентрации. Тева вывела на американский рынок две дозировки: 150 и 300 мг. С тех пор от пациентов стали поступать различные жалобы, начиная от «невинного» плохого запаха, до тяжелых: усиления депрессии, судорог и самого грозного осложнения депрессии — суицида. Многократные обращения медицинских работников в FDA делу не помогали (говорить о том, что Тева отвергала все обвинения, излишне). Вместе с тем все же агентство запустило расследование и сообщило обращающимся, что в исследованиях биоэквивалентности изучена только меньшая дозировка (150 мг, а не 300) и что агентство считает препараты сопоставимыми, хотя налицо была клиническая несопоставимость.
Весь пересмотр данных агентство провело за «закрытыми дверями», не вынося вопрос на публичное обсуждение, причем само расследование рекламаций на качество и безопасность состояло в перепроверке старых отчетов об исследованиях биоэквивалентности без дополнительных испытаний на растворение. Однако ситуация была столь критичной, что через несколько лет FDA была вынуждена провести спонсируемое им исследование биоэквивалентности для дозировки 300 мг, в котором выяснилось, что время достижения максимальной концентрации на фоне оригинального бупропиона (Веллбутрин) —5 часов, тогда как на фоне «генерика» Тевы — 2 часа. Такой профиль высвобождения (называемый «сбросом дозы») очень хорошо объяснял клиническую картину у многих пациентов. После получения этих данных Тева отозвала свой препарат с рынка, а высокопоставленный служащий FDA, контролировавший и затягивавший все расследование, уволился из агентства и стал регуляторным директором Тевы.
Это дело, как и все дело Ранбакси, а также другие подобные, но менее известные разбирательства показали, что FDA — закрытая контора, которая не будет давать информацию и проводить расследование, если это угрожает ее корпоративным интересам.
В то же время внезапно участились случаи смерти пациентов, получавших свиной гепарин. Число жертв исчислялось десятками, а несмертельных серьезных нежелательных реакций было и того больше. Началось расследование в Конгрессе. Длительные разбирательства позволили установить причину — ряд препаратов гепарина содержали примеси гиперсульфатированного хондроитинсульфата (ГСХС), который приводил к чрезмерной антикоагулянтной активности препарата и повышению частоты жизнеугрожающих кровотечений. Один человек в этой ситуации потерял свою семью: жену и сына, которые пали жертвами такого некачественного гепарина.
Разбирательства сначала привели FDA к китайским производителям и позволили вскрыть причину: для повышения выхода гепарина, получаемого из слизистой оболочки свиней, к нему прибавляли гепаринсодержащее сырье из крупного рогатого скота — источник токсичного контаминанта. С тех пор контроль качества гепаринов в числе прочего предполагает скрининг на ГСХС. Интересно отметить, что установить виновную производственную площадку удалось не сразу, поскольку инспекторы сначала проверили не тот завод: система адресов в Китае запутана для неискушенных иностранцев, а китайские власти инспекторам FDA поддержку не оказывали. Более того, многие китайские заводы, производящие лекарственные вещества и другие фармацевтические ингредиенты на экспорт, работают в Китае в качестве химических (а не фармацевтических) производств, и поэтому подвергаются гораздо менее строгим проверкам.
Параллельно с этими событиями многолетняя бюрократическая машина FDA в 2010 г. довела дело до судебного разбирательства, то есть спустя около 5 лет после того, как Динеш Такур впервые написал в агентство о злодеяниях компании. И даже тогда все шло ни шатко ни валко. «Почему же FDA так старается предотвратить крах зарубежной индийской компании, у которой вообще нет достоверных данных?» — задавались вопросом прокуроры, сопровождавшие дело со стороны Департамента юстиции. Однако поступавшие все новые и новые порции данных двигали расследование и оформление дела вперед.
По результатам инспекций, свидетельствам многочисленных информаторов, которых данный процесс воодушевил, выяснилось, что Ранбакси для проведения исследований биоэквивалентности, испытаний на стабильность, испытаний на растворение и других тестов на качество, вкладывала в капсулы раскрошенные оригинальные препараты. Компания с легкостью подделывала хроматограммы. Ее работники срисовывали тесты на растворение, доступные в открытых источниках. Так, одна из бывших работниц Ранбакси, отвечавшая за фармаконадзор и пришедшая в компанию из Илай Лили (Eli Lilly), делилась, как она была восхищена искусности Ранбакси в разработке, когда увидела полное совпадение профилей растворения одного из препаратов компании с растворением оригинального препарата. После того как ей попался идентичный профиль растворения на другой препарат у нее стали появлятся подозрения; на третьем, четвертом и пятом препаратах она поняла, куда она попала, поэтому быстро покинула Ранбакси.
Ранбакси не гнушалась запугивать людей и даже угрожало прямыми физическими расправами тем, кто ей мешает.
На переговорах Ранбакси говорила, что «хитрить» — это культура Индии. В этой стране людям тяжело живется, поэтому приходится придумывать различные ухищрения для обхода законов. При этом административные барьеры в стране столь сложные и бессмысленные, что никто не утруждает себя их исполнением, все «хитрят» и «крутятся, как могут». Для служащих FDA же было очевидно, что культура вранья, сложившаяся в этой стране, вынуждает их сомневаться в качестве всех поступающих оттуда препаратов.
Одной из причин, почему FDA не спешила расправиться с Ранбакси (помимо внутрикорпоративных интересов и тесных связей некоторых служащих с отраслью), было сильное давление, которое испытывало агентство со стороны вышестоящих властей (Конгресса и Белого дома) и общественности по обеспечению доступности дешевых генериков, поскольку в США лекарственная помощь стоит бюджетам и обществу баснословных денег.
В частности, примерно в это же время заканчивалась патентная защита на оригинальный аторвастатин — «супер блокбастер» от Пфайзер для снижения холестерина в крови, который ежегодно приносил компании несколько миллиардов долларов. Ранбакси в свое время удалось раньше других подать заявление на регистрацию, чем она заслужила право продавать его в течение 180-дней без какой-либо конкуренции со стороны других генериков — очень заманчивая цель для любой компании, поскольку одни только продажи воспроизведенного аторвастатина сулили Ранбакси доходы, исчислявшиеся сотнями миллионов долларов.
В результате FDA, чтобы позволить Ранбакси заработать денег для выплаты штрафа, решила одобрить досье компании и выдать разрешение на продажу. Однако агентство обязало производить препарат на заводе, располагавшемся в США, в штате Нью-Джерси, который находился «под колпаком». Через неделю после того, как Ранбакси получила разрешение, она направила в FDA заявление о внесении изменений в регистрационное досье с целью переноса производственной площадки из Нью-Джерси в Индию. По административным причинам и под сильным нажимом Конгресса и общества, которые не знали о тяжелых взаимоотношениях агентства с Ранбакси (и состоянии производства лекарств в Индии в целом) FDA согласовала перенос производства — компания заработала деньги на штраф.
В 2012 г. состоялся суд, по результатам которого Ранбакси выплатила 500 млн. долл., из которых 46 млн. долл. отошли Динешу Такуру, полагавшиеся ему на основании Закона о мошенничестве (False Claims Act). Другим крупным [96 млн. долл.] получателем выплат на основании этого закона в области фармацевтики является Шерил Экард (Cheryl Eckard), раскрывшая недобросовестные производственные практики GlaxoSmithKline, которые имели место на заводе компании в Пуэрто-Рико, работавшем без обеспечения стерильности, с сильной контаминацией лекарств и т. д.
Дело Ранбакси велось за закрытыми дверями, поэтому о проблемах знали только в FDA и самой компании. Внешне Ранбакси казалась крупной успешной компанией, спасителем здравоохранения, образцом гуманизма, но умеющей вести бизнес. Примерно в 2008–2009 гг. ею заинтересовалась японская Дайичи Санкьё, а в 2010 г. приобрела контрольный пакет. Никакие аудиты не позволили руководству Дайичи Санкьё узнать истинные нарушения Ранбакси и те проблемы, из-за которых ее прессовала FDA. Отчет о внутреннем аудите (SAR) стал доступен инвестору, вложившему в индийского гиганта 2 млрд. долл., только после суда в США, когда Дайичи Санкьё узнала истинное положение вещей. И даже после этого Малвиндер Сингх все отрицал.
Вся эта история привела FDA к осознанию, что проведение инспекций зарубежных производителей в уведомительном порядке является напрасной тратой ресурсов, поэтому она вела переговоры с индийскими властями о создании в стране собственного офиса для инспектирования. И такое разрешение она получила. Одним из первых инспекторов индийского офиса стал Питер Бейкер (посмотрите его профиль на LindedIn). Бейкер был одаренным инспектором, можно сказать сыщиком: он умел находить то, что пропустили другие. У него было чутье на нарушения: даже легкие на первый взгляд «странности», на которые бы другой не обратил внимание, нередко приводили к вскрытию им колоссальных нарушений.
В частности, инспекция Бейкером завода компании Вокхарт в 2013 г. показала, что данные на инсулин отсутствуют или не соответствуют фактически производимому препарату. В частности, он обнаружил секретные линии производства с черными металлическими (!) включениями. Препарат не продается в США, как отмечает автор, но до сих пор на рынке других стран (арабские страны, страны Африки, Россия) [от себя: это тот же самый инсулин, в регистрации которого в том же 2013 г. отказало Европейское агентство по лекарствам, поскольку данные о его разработке не соответствовали препарату, который производится компанией в настоящее время: отсутствовали данные о валидации производства препарата, который бы соответствовал препарату, изученному в опорных клинических исследованиях (т. н. в глюкозных клэмпах); для наших экспертов по качеству это не явилось препятствием].
В другом случае Бейкер наткнулся на неправильно укупоренный и тем самым нестерильный гемцитабин — противоопухолевое средство для парентерального введения; препарат шел на американский рынок.
Что характерно, масштабные нарушения со стороны индийских компаний продолжались и после того, как Ранбакси была оштрафована на огромную сумму. В ходе своего пребывания в Индии Бейкер столкнулся с уничтожением данных прямо на его глазах, бегством работников, пойманных с документальным подтверждением нарушений, мочой в производственных зонах, обнаружением гнездовий птиц, змей, нашествием обезьян на производственные площадки, полчищами мух в стерильных производствах; секретными формуляционными линиями. и т. д. Бейкера удивляло, что заводы располагали достаточными техническими и инфраструктурными возможностями, но тратили их на подделку как самих лекарств, так и документации.
По этой причине производители делали все возможное, чтобы заранее выяснить, куда будут направляться инспекторы, а также принимали меры для воспрепятствования ходу инспекции. В частности, были случаи, когда инспекторам подмешивали снотворное, в ответ перед посещением площадки инспекторы стали продумывать план экстренной эвакуации. Были случаи, когда для отправки инспекционных находок в головной офис FDA по вызову инспекторов приезжали подставные работники DHL. Были случаи, когда инспекторы обнаруживали, что их номера в отелях прослушиваются, в результате инспектируемые лица были готовы к заранее продуманному плану инспектирования. Работники индийского офиса FDA также допускали утечку информации, поэтому инспекторы вообще перестали их информировать, а потом и отказались от идеи индийского офиса. Были неоднократные попытки подкупа, вероятно, где-то успешные: несмотря на отсутствие прямых доказательств агентство сильно подозревало инспектора Мурала Гавини, этнического индуса, в сговоре с индийскими производителями. Как ни странно, FDA было очень тяжело избавиться от него.
Инспекторы стали прилетать на инспекции по дипломатическим каналам, возложив все мероприятия по организации инспекций на сотрудников государственного департамента США. В итоге компании стали вести мониторинг аэропортов и отелей для отслеживания прибытия инспекторов.
Однажды Бейкер с напарником прибыли на инспекцию, о проведении которой сообщили за несколько дней до ее начала. Первым днем инспекции должен был быть понедельник, однако приехали они туда в воскресенье, никому заранее не сообщив об этом. Завод был полон работников, которые дружно уничтожали документацию, мыли помещения и другим образом заметали следы. Окна в стерильных производственных зонах были открыты настежь, везде летали мухи, люди ходили босиком. Инспекторов распознали не сразу — увидев двух людей европейской внешности, сотрудники завода подумали, что это очередные аудиторы, поэтому продолжали свою деятельность как ни в чем не бывало.
В другом случае Бейкер с напарником нашли лабораторию с идеальными документированными результатами, которая однако вообще ничего реально не тестировала и содержалась производителем только ради фабрикации результатов испытаний; на дворе стоял 2014 год.
Хорошим способом понять что к чему Бейкер считал разговор с рядовыми работниками, у которых можно было выудить ценнейшую информацию о нарушениях. Как-то поймав одного такого рабочего, который пытался скрыть очередную порцию документов, тот взмолился, что не может признаться, ибо боится потерять работу, которую в Индии очень тяжело найти. По этой причине приходиться идти на нарушения и на многое закрывать глаза. Бейкер понимал, что нищенские условия рабочих, высокая неграмотность, социальная и трудовая незащищенность, страх потерять работу вседозволенность для власть предержащих создавали оптимальные условия для масштабных нарушений.
В одном из интервью в 2015 г. глава индийского регулятора открыто обмолвился, что если они будут проводить инспектирование по западным стандартам, то Центральная организация по контролю стандартизации лекарств — лекарственный регулятор Индии — будет вынуждена закрыть почти все фармацевтические заводы, располагающиеся в стране.
Бейкер отмечал, что инспекторы фактически обучают индийских производителей тому, как можно нарушать и не быть пойманным; никто и не помышлял начинать производить лекарства по правилам. Почти все лекарства имели ту или иную степень брака, причем более некачественная продукция сбывалась на развивающиеся рынки. Серии, не выдержавшие испытания, на одном из индийских заводов, располагавшегося к югу от Хайдерабада и производящего препараты для американского рынка, отправлялись по признанию самого руководства завода на украинский рынок (глава 26). Альтернативные производственные линии — обычная практика. Если страна предъявляет высокие требования к качеству, то препараты выпускаются на «хорошей линии»; если требования страны к качеству лекарств низкие, то предусмотрены отдельные линии для экономии ресурсов. Худшая, бракованная и отвергнутая продукция (даже по индийским меркам) отправлялась на три основных рынка: в Экваториальную и Субэкваториальную Африку, Южную Америку и Восточную Европу. Руководство какой-то из индийской компаний так и говорило: каким бы плохим ни было «лекарство», всегда найдутся его покупатели.
Примечательна ситуация в Африке. В Уганде врачи, работавшие по линии «Врачей без границ» в 2013 г. стали отмечать, что некоторые лекарства для лечения инфекционных гнойно-септических заболеваний не помогают их пациентам. Некоторые даже подозревали возникновение новых патогенов, однако более опытные коллеги давно знали, в чем может быть дело. Стоило пациенту дать оригинальное лекарство или неиндийский генерик, как он почти наверняка шел на поправку, однако такие лекарства из-за их дороговизны держали в качестве резерва. Подобное «чудодейственное» выздоровление в Уганде прозвали «эффектом Лазаря». Основной проблемой в случае противомикробных лекарств было меньшее, чем положено, содержание активных ингредиентов, ибо это не только угрожало конкретному пациенту, но и стало одной из причин — согласно докладам ВОЗ — формирования широкой антибиотикорезистентности. Однако на ситуацию в Уганде было достаточно тяжело повлиять, поскольку препараты закупались без какого-либо контроля. Лишь в 2016–2017 гг. в стране заработала лаборатория по контролю качества лекарств, находящихся на рынке.
Многие служащие FDA признавались автору книги, что после всего обнаруженного они стали принимать все возможные меры, чтобы избегать назначения себе и своим семьям генериков из Индии, а некоторые — рубежные генерики вообще, о чем они даже заявляли публично на слушаниях в Конгрессе. На одном из заседаний, они сокрушались: «Если бы только люди вникли и осознали, какая это опасность и мошенничество, они бы не принимали генерики, производимые таким образом».
В 2015 году Бейкер покинул Индию и переехал в Китай для инспектирования производителей активных фармацевтических ингредиентов. Самая первая инспекция в Китае была на контрактной производственной площадке Пфайзер. Компания работала с китайским производителем для получения аторвастатина вот уже 3 года. Нареканий со стороны отдела обеспечения качества Пфайзер не было, поэтому доверия к китайским производителям было больше. В первый же день инспектирования Бейкер направился в аналитическую лабораторию по контролю качества. В университете он изучал китайский, поэтому попросив сотрудника лаборатории предоставить доступ к компьютеру, он стал искать иероглифы, обозначавшие «пробный анализ» и т. п. В первый же день он вскрыл систему двойного документооборота, о которой в Пфайзер даже не подозревали! Через год компания прекратила сотрудничество с заводом.
На другом из заводов Бейкер к своему удивлению обнаружил шредер посреди производственного цеха. Само по себе это не преступно, но сеет подозрения. В результате на этой производственной площадке также были обнаружены критические ошибки. На повторной инспекции шредер исчез из цеха, но обнаружился в итоге в аналитической лаборатории. Из других находок часто встречались не документируемые «пробные» испытания, незарегистрированное контрольное оборудование (хроматографы) и т. п.
До Бейкера китайские производители были крепким орешком для контролеров из Европы и Северной Америки. Сами же китайцы, по описанию автора книги, составленной ей на основании разговоров с представителями регуляторов, американскими производителями и информаторами с китайских заводов, считали чуть ли не своей обязанностью водить за нос проверяющих, приезжающих с Запада. Были случаи, когда под видом разных заводов инспекторов из разных стран возили на один и тот же. Была практика демонстрации образцовых производств и лабораторий, в реальности никогда не производивших лекарства и т. д. Ситуация была очень похожа на положение вещей в Индии.
Китайские производители, до того особо не встречавшие проблем с одурачиванием инспекторов, стали сильно боятся Бейкера. Тот же один за другим выдавал отчеты по форме 483 с заключением OAI. Форма 483 — форма отчета об инспекции FDA; OAI— official action indicated (показано принятие официальных мер) — оборот, означающий запрет заводу поставлять продукцию на рынок до устранения недочетов. Тогда как VAI — voluntary action indicated (показано принятие добровольных мер) — оборот для обозначения небольших недочетов, устраняемых без запрета выпуска на рынок. Наконец, NAI (no action indicated) — принятие мер не требуется.
Однако такое больше число OAI от Бейкера в отношении китайских заводов отнюдь не радовало высшие чины FDA, наоборот, это было проблемой. Конгресс и Администрация президента оказывали на FDA давление по обеспечению доступа к дешевым лекарствам, что предполагало увеличение числа производителей (и Китай вместе с Индией здесь занимал ведущие позиции), а не их сокращение. Многие предложения Бейкера о согласовании OAI отклонялись и снижались до VAI, что позволяло заводам дальше поставлять бракованную продукцию на рынок США.
Несмотря на то что Бейкер был героем среди рядовых инспекторов, в агентстве не все радовались его успехам и достижениям. Руководство FDA говорило, что они не могут требовать от всех своих служащих такого рвения в работе (в том числе ковыряние в мусорках), инспектирования во внеурочное время и т. д.
Вместе с тем в Евросоюзе он был очень популярен среди инспекторов: его регулярно приглашали, чтобы обучить европейцев подходам Бейкера к выявлению недобросовестности при производстве и контроле на китайских и индийских производствах (от себя: на официальном YouTube-канале EMA есть хороший видеокурс по тренингу инспекторов:
, в том числе как избегать проблем с агрессивными производителями). Кроме того, аудиторы в области GMP признавались, что их доходы существенно возросли благодаря Бейкеру, поскольку спрос на предварительный контроль со стороны производителей сильно увеличился.
Однако несмотря на все заслуги Бейкера, корпоративные интересы FDA все же возобладали, и 2018 г. он был отозван из Китая и переведен в чилийский офис агентства. Однако там ему не давали каких-либо серьезных заданий, поэтому он покинул агентство в том же году и начал работать GMP-аудитором.
Смотря на ситуацию с зарубежными генериками, продаваемыми на американском рынке, интересно также взглянуть на генериковую отрасль самих Штатов.
Одним из основных игроков в стране и флагманом надлежащих практик в этой области была компания Mylan. Именно работники Mylan в 1988 г., то есть спустя 4 года после узаконивания сокращенного механизма одобрения генериков в США (закон Хэтча-Ваксмана), вскрыли масштабную коррупцию в офисе воспроизведенных лекарств FDA. Office of Generic Drugs, OGD — подразделение FDA, занимающееся экспертизой генериков и составляющее те самые препаратспецифичные монографии на генерики, число которых приблизилось к 1700; с точки зрения научного потенциала людям оттуда нет равных среди регуляторов. Однако в тот год несколько служащих OGD FDA были уличены в почти неприкрытых взятках в виде дорогих путешествий, подарков и т. д., которыми они вознаграждались за выдачу разрешений конкурентам Mylan’а. Например, в случае одного из экспертов FDA улики были обнаружены в мусорном ведре его дома: это были чеки на покупки, которые служащий не смог бы приобрести при его уровне заработка на госслужбе.
Предпосылки для коррупции были созданы самим агентством, по предложению которого, в рамках закона Хэтча-Ваксмана была согласована возможность предоставления 180-дневной рыночной исключительности первому зарегистрированному генерику. Это норма имела вполне логичное обоснование: вывод первого генерика может так или иначе сопровождаться нарушением патентных прав оригинатора. Тот, свою очередь, конечно же, будет защищать свои интересы в суде и может победить, в связи с чем первый разработчик может понести существенные потери. Для вознаграждения риска, на который идет первый разработчик генерика, и была введена норма о 180-дневной исключительности первого генерика.
Поскольку дата истечения патента в целом была известна (она указывается в Оранжевой книге), довольно регулярно возникали ситуации, когда на парковке перед офисом воспроизведенных лекарств FDA еще за несколько дней до предполагаемой даты возможной подачи заявления на регистрацию генерика (т. н. ANDA — сокращенное заявление на новое лекарство) собирались очереди, а в день подачи иногда даже случались потасовки между представителями разных компаний. Однако все на этом не заканчивалось, поскольку принятым считалось только существенно полное досье (substantially complete ANDA). Разумеется, полнота досье выяснялась служащими FDA позднее. Такая неразбериха и предоставление 180-дневной исключительности создавали почву для манипуляций и злоупотреблений, приведших к кризису 1988 г. Лишь 1992 г. FDA исправила положение вещей, решив предоставлять 180-дневную исключительность всем компаниям, первым подавшим ANDA в один и тот же день.
Благодаря этой истории Майлэн снискала славу этичной и честной компании, отстаивавшей принципы добросовестного ведения бизнеса. Однако в начале нового тысячелетия компания также начала испытывать конкуренцию со стороны зарубежных генериковых компаний и принимала соответствующие меры. Одной из таких мер был наем Юсуфа Хамида (см. выше) из индийской Циплы, идейного вдохновителя индийского генерического «чуда», в качестве специалиста по фармацевтической разработке для улучшения квалификации Mylan в этой сфере. Юсуф Хамид действительно принес новые знания и позволил Mylan многого добиться с точки зрения расширения продуктового портфеля. Сам он постепенно добрался до правления американской компании — нечастое явление для иностранца.
Однако столь стремительный успех дался компании не на пустом месте: вместе с собой Хамид привел свою индийскую команду разработчиков. Хамид и его команда, пусть открыто и не прибегали к индийским методам, но все же ряд сотрудников стал отмечать, что целью Хамида была регистрация максимального числа препаратов (от этого в том числе зависел его заработок), при этом высокое качество, постоянство производства и стабильность препарата стояли далеко не на первом месте, поэтому бракованная продукция перестала быть редкостью, участились отзывы продукции с рынка.
Кроме того, в правление компании вошла дочь одного из сенаторов Конгресса, что также упрочило позиции компании на политической арене, поэтому ряд проблем производства и качества стали решаться политическими мерами. Это также не пошло на пользу имиджу Mylan. В результате компания, осознав, в какой ситуации она оказалась, в 2018 г. избавилась от Хамида и его команды, равно как и от дочки сенатора и пытается теперь восстановить свою пошатнувшуюся репутацию.
Все произошедшие за это время пертурбации с генериками вынудили Кливлендскую клинику (Cleveland Clinic, штат Огайо) — одного из ведущих академических медицинских центров страны, являющегося, возможно, самым взыскательным покупателем лекарств в США, прийти к выводу, что нужно избегать определенных фармацевтических производителей. При этом простые люди должны получить возможность принимать информированные решения, основанные на знании рисковых производителей.
Сегодня Ранбакси больше нет. В 2014 г. очередной информатор, сообщил материнской компании — японской Дайичи Санкьё, что персонал Ранбакси подмешивал в активные ингредиенты дешевые некачественные загрязненные полупродукты, вел двойную документацию (настоящую и для регуляторов), отбеливал желтые из-за примесей таблетки, которые должны были быть белыми, прятал улики сначала под потолочными плитами, а потом выбрасывал в реку. Дайичи Санкьё решила избавиться от Ранбакси и продала ее индийской Сан Фармасьютикалз: бренд Ранбакси перестал существовать. (Однако если поискать «Ранбакси» в госреестре лекарственных средств, то обнаружится, что за этой несуществующей компании все еще числится ряд лекарств с действующими регистрационными удостоверениями).
Более того, Дайичи Санкьё подала в суд на самого Малвиндера Сингха в международный арбитраж в Сингапуре, отсудив у него 850 млн. долл. за недобросовестные практики. Даже Верховный суд Индии, защиты которого просил Сингх, оставил в силе постановление Сингапурского суда. Сам Сингх все отрицал до последнего и продолжает выставлять жертвой себя. (В татарском языке есть поговорка в отношении подобных людей, которую можно перевести как «давать под зад, глядя в глаза»).
Однако исчезновение Ранбакси не означает, что исчезли люди. Представителей бывшего топ-менеджмента компании, известных своими навыками создания досье ещё до завершения фармацевтической разработки, можно признать одними из лучших фальсификаторов в фармацевтической отрасли. Теперь они проникли в другие компании.
Казалось бы, что история закончилась, враг побежден. Однако в 2016 г. на весь мир прогремел запрет Евросоюзом около 700 лекарств, оценка биоэквивалентности которых проводилась в одном из клинических центров Индии: французские GCP-инспекторы вскрыли подделывание ЭКГ. На основании этого они усомнились во всех остальных данных, полученных в этом исследовательском центре. FDA какие-то меры приняла, но полностью препараты не запретила.
Уже в 2018 г. Европа вскрыла масштабную загрязненность генериковых антагонистов рецепторов ангиотензина II («сартанов») генотоксичными примесями — нитрозаминовыми производными. При этом виновная Чжэцзян Хуахай (опять же посмотрите на сартаны в нашем госреестре) признала, что процесс, приводивший к образованию таких примесей, действовал с 2012 г. Новость из Европы застала FDA врасплох, хотя не должна была: еще в 2017 г. во время инспекции было выявлено зашкаливание примесей и инспекторы FDA предлагали OAI, но функционеры агентства снизили его до VAI и забыли про дело.
Послесловие
История с индийскими и китайскими производителями не стала для меня открытием, скорее, послужила подтверждением (довольно детальным и с яркими примерами) того, что я (как и многие другие) давно подозревал. Однако мое мнение об FDA как эталоне обеспечения качества и регулирования лекарств сильно пошатнулось. Вместе с тем отмечу, что с научной и инспекционной точки зрения агентство (пока) все равно является мощнейшим; политика вносит свои уродливые коррективы в принятие решений. Европа же на этом фоне выглядит довольно порядочно, хотя без подобных расследований сложно говорить, какова внутренняя кухня. Вместе с тем подозреваю, что европейцы честнее, потому что это союз 28 (пока что) государств, поэтому скрыть нарушения гораздо сложнее. Более того, их можно признать ведущими в области обеспечения прозрачности.
Возвращаясь к нам: теперь требование о повторении исследований биоэквивалентности в России не кажется столь уж вредным, равно как и требование, чтобы наш инспекторат выезжал на зарубежные производства. Безусловно, хорошо бы наладить взаимодействие с ЕС и США по этой линии, но также важно повышение уровня наших инспекторов, обучение их навыкам сыска. Вместе с тем здесь важна рьяность и по отношению к собственным производителям. На фоне этой истории вообще можно попробовать поднять отечественную генериковую отрасль, если нацелить ее на экспорт в ЕС и США: как минимум у нас нет обезьян, а зимой еще и мух.
Фармацевтические разработка, изыскания и производство — сложные наукоемкие технологические процессы, требующие больших интеллектуальных вложений (иначе и быть не может, поскольку мы вмешиваемся в сложные процессы человеческой биохимии и генетики), поэтому невозможно одновременно достичь высокого качества, дешевизны и честности.
Что касается задач (государственного) контроля: подозрение в случае ряда компаний и стран должны трактоваться против них, то есть в пользу наших пациентов!
Это, подобное и другое про лекарства на Телеграм-канале Мета-Ф.
P.S. Спасибо Vasiliy Vlassov, что порекомендовал прочесть.
Добро всегда накажет Зло, поставит его на колени и жестоко убьет.
-
 Андрей Эдельвейсс
Андрей Эдельвейсс
Автор темы - Трактирщик
- Сообщения: 8358
- Зарегистрирован: 29 май 2015, 19:55
- Награды: 5
- Откуда: СССР
- Род занятий: колымим
- :




- Благодарил (а): 1099 раз
- Поблагодарили: 2392 раза
- Status: Не в сети

Миллионеры в белых халатах: сколько фармкомпании платят российским врачам
Не менее 42,4 тыс. российских врачей, по подсчетам РБК, получили в 2018 году от фармацевтических компаний более 3,3 млрд руб. Вознаграждение 29 специалистам превысило 1 млн руб. каждому
Фото: Кирилл Кухмарь / ТАСС
РБК изучил отчеты 43 фармацевтических компаний о так называемой передаче ценностей российским специалистам здравоохранения в 2018 году — выплатах врачам за участие в научных конференциях, компенсациях расходов на поездки и проживание, вознаграждениях за консультации и т.п.
Такие отчеты компании, входящие в Ассоциацию международных фармацевтических производителей (AIPM; она, в свою очередь, является членом Европейской федерации фармацевтической промышленности и ассоциаций, EFPIA), публикуют четвертый год подряд. Прозрачность, по замыслу отраслевых объединений, повысит «взаимную ответственность и этичность взаимодействия между фарминдустрией и медицинским сообществом», в результате чего выиграют и пациенты.
Ключевые факты из отчетности и рейтинг врачей, получивших в прошлом году наибольшее вознаграждение, — в обзоре РБК.
Отчетность фармкомпаний в цифрах
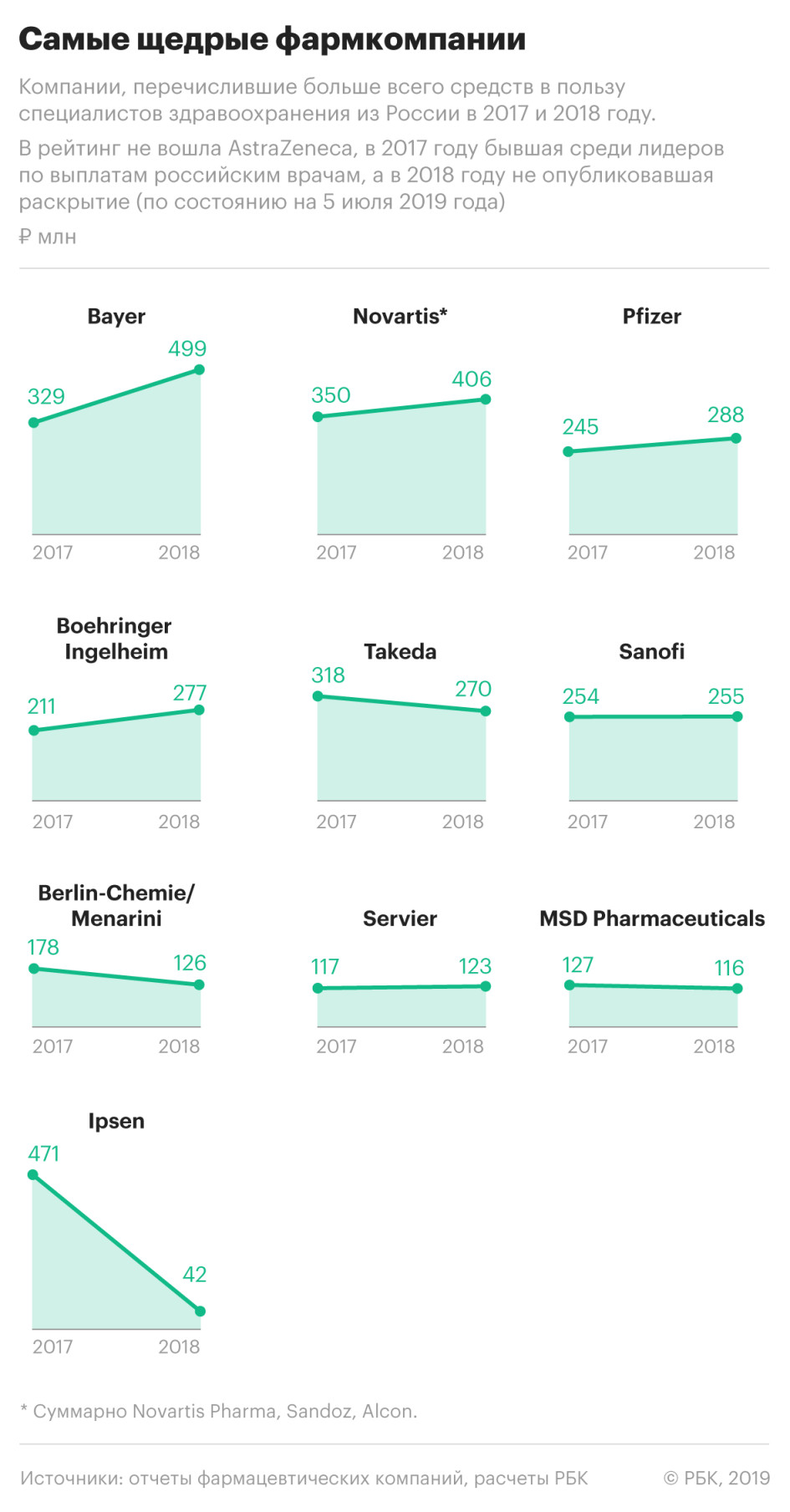
Общая сумма выплат врачам у отчитавшихся за 2018 год компаний — около 3,3 млрд руб.
Количество специалистов, давших согласие на раскрытие информации о собственном вознаграждении, — 9,4 тыс. человек. Их число по сравнению с 2017 годом снизилось.
Общая сумма выплат таким специалистам — 607,4 млн руб. Средний размер выплаты — от 24 тыс. до 252 тыс. руб. в зависимости от компании.
Количество специалистов, не согласившихся на раскрытие информации, — не менее 33 тыс. человек. Точное количество указать невозможно, поскольку из отчетности многих компаний нельзя сделать вывод, получил ли врач больше одной выплаты или нет.
Общая сумма выплат анонимным специалистам — 2,7 млрд руб. Средний размер выплаты — от 10 тыс. до 310 тыс. руб. в зависимости от компании.
Число врачей в 2018 году, по данным Росстата, — 560,2 тыс. человек.
Средняя по России ежемесячная зарплата врача, по данным Росстата, — 75 тыс. руб.
На сайте AIPM членами ассоциации указаны 63 компании (с учетом дочерних структур). Дедлайном при публикации материалов традиционно является 30 июня. По состоянию на 4 июля на сайтах компаний — членов AIPM были доступны лишь 43 отчета. Среди производителей, которые ранее раскрывали информацию, но в этом году в срок ее не предоставили, — Allergan (ее покупает AbbVie), AstraZeneca, Ferring Pharmaceutical, Merz Pharma, Zambon Group. На запросы РБК в этих компаниях на момент публикации не ответили.
Больше всего врачам в 2018 году перечислила немецкая Bayer — 498,6 млн руб. Количество медиков, получивших выплаты, может составлять от 3,9 тыс. до 7 тыс. человек. Конкретная информация приведена только в отношении 74 человек.
Наименьший размер выплат в 2018 году — 1,9 млн руб. — у американской Celgene. Деньги получили 24 специалиста, из которых лишь о семи информация раскрыта.
В 14 раз — с 3,1 млн до 44,2 млн руб. — в прошлом году выросли платежи у Amgen. В 2018 году эта американская компания сотрудничала с 498 врачами, известны имена 84 из них.
Больше всех снизился бюджет у французской Ipsen: с 471,2 млн руб. в 2017 году до 41,9 млн руб. в 2018-м. В прошлом году эти деньги получили не менее 583 специалистов, из них 558 разрешили опубликовать подробную информацию о своем вознаграждении.
За что фармкомпании платят врачам
Максимальные выплаты врачам представляют собой преимущественно вознаграждения за оказание услуг и консультирование, свидетельствуют проанализированные РБК отчеты.
За этой формулировкой может скрываться все что угодно: разработка протоколов исследований или, например, цикл лекций, указывает главный врач столичной Городской клинической больницы им. С.С.Юдина Денис Проценко. В основном такие выплаты от компаний — это не разовые отчисления, а гонорары за чтение лекций и участие в научных мероприятиях, которые проходят при поддержке фармкомпаний, объясняет заведующий отделением реанимации и интенсивной терапии московской Городской клинической больницы № 29 Алексей Эрлих.
Закон «Об основах охраны здоровья граждан в РФ» не разрешает медицинским работникам принимать денежные средства от фармкомпаний и их представителей. Но под этот запрет не попадают гонорары за проведение клинических исследований и испытаний и вознаграждения за педагогическую и научную деятельность.
Рейтинг врачей
По итогам 2018 года у 29 российских врачей размер платежей от фармкомпаний превысил 1 млн руб. Лидером рейтинга стала Татьяна Пестова, специалист-репродуктолог из Челябинска. От Merck за «оказанные услуги и консультирование» она в прошлом году получила почти 2,7 млн руб., еще 164 тыс. руб. (из них 102 тыс. — компенсация транспортных расходов) ей перечислила Abott. Связаться с Пестовой в пятницу, 5 июля, не удалось.
Главному внештатному эндокринологу министерства здравоохранения Краснодарского края Инне Кудлай та же Merck, как указано в ее отчете, перечислила за услуги и консультации 2,6 млн руб. Еще 7 тыс. руб. в качестве компенсаций транспортных расходов этот врач получила от Ipsen. Но в беседе с корреспондентом РБК Кудлай заявила, что вообще не работает ни с Merck, ни с Ipsen. «Я была бы очень рада, если бы была таким богатым человеком», — ответила Кудлай. Она перестала отвечать на звонки корреспондентов РБК после того, как ей были отправлены отчеты фармкомпаний.
Отказался комментировать заявленные в отчетности венгерской Egis почти 2,2 млн руб. директор терапевтический клиники и заведующий кафедрой терапии, клинической фармакологии и скорой медицинской помощи МГМСУ им. А.И.Евдокимова Аркадий Верткин.
Профессор кафедры молекулярной фармакологии РНИМУ им. Н.И.Пирогова Александр Духанин подтвердил РБК, что сотрудничал в прошлом году с Pfizer и Sanofi, и допустил, что мог получить выплаты и от других фармкомпаний. Но он усомнился с заявленном размере выплат: почти 78 тыс. руб. за оказанные услуги и консультации от Pfizer и 1,3 млн руб. (с учетом 332 тыс. руб. компенсации транспортных расходов) от Sanofi. «Предполагаю, что включены не только гонорары, но расходы на перелеты и проживание, потому что сумма получается какая-то астрономическая, — заявил Духанин. — Поскольку я преподаватель, научный сотрудник, а не практикующий врач, то эти суммы уходят на образовательную работу».
Кардиоревматолог профессор Илья Егоров (на личном сайте называет себя «постоянным медицинским экспертом» «Первого канала», «России 1», «ТВ Центра» и НТВ») рассказал, что для Egis он делает «буквально несколько выступлений в год», а для Merck — 10–12. Компании отчитались о перечисленных Егорову соответственно 723 тыс. и 1,3 млн руб. (из них 63 тыс. — компенсации транспортных расходов). В этих цифрах указан не только гонорар лектору, но и другие расходы, убежден Егоров.
«У фармкомпаний есть свой интерес — конечно, они приглашают лекторов, которые в своих выступлениях так или иначе будут говорить про их препараты. Но 20 лет назад, когда к нам только пришла эта форма бизнеса, это была чистая реклама, а потом стало понятно, что это неинтересно врачам, — вспоминает Егоров. — И в последнее десятилетие лекторы, которые работают с фармкомпаниями, понимают, что они должны дать своим слушателям вкусную, яркую, актуальную тему — обучение правильной диагностике, разговору с пациентом».
Сейчас реклама препаратов стала настолько непопулярной, настолько невостребованной, что о них говорится вскользь, в контексте, уверяет Егоров.
Связаться с другими фигурирующими в рейтинге врачами не удалось.
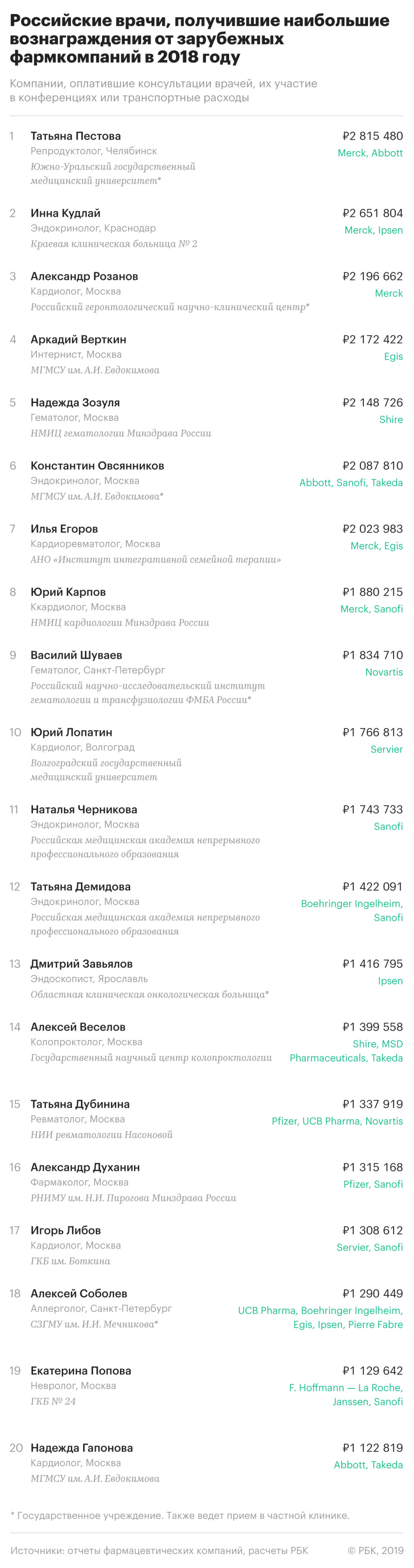
Подробнее на РБК:
https://www.rbc.ru/rbcfreenews/5d218f109a794781e30c6b93
Не менее 42,4 тыс. российских врачей, по подсчетам РБК, получили в 2018 году от фармацевтических компаний более 3,3 млрд руб. Вознаграждение 29 специалистам превысило 1 млн руб. каждому
Фото: Кирилл Кухмарь / ТАСС
РБК изучил отчеты 43 фармацевтических компаний о так называемой передаче ценностей российским специалистам здравоохранения в 2018 году — выплатах врачам за участие в научных конференциях, компенсациях расходов на поездки и проживание, вознаграждениях за консультации и т.п.
Такие отчеты компании, входящие в Ассоциацию международных фармацевтических производителей (AIPM; она, в свою очередь, является членом Европейской федерации фармацевтической промышленности и ассоциаций, EFPIA), публикуют четвертый год подряд. Прозрачность, по замыслу отраслевых объединений, повысит «взаимную ответственность и этичность взаимодействия между фарминдустрией и медицинским сообществом», в результате чего выиграют и пациенты.
Ключевые факты из отчетности и рейтинг врачей, получивших в прошлом году наибольшее вознаграждение, — в обзоре РБК.
Отчетность фармкомпаний в цифрах

Общая сумма выплат врачам у отчитавшихся за 2018 год компаний — около 3,3 млрд руб.
Количество специалистов, давших согласие на раскрытие информации о собственном вознаграждении, — 9,4 тыс. человек. Их число по сравнению с 2017 годом снизилось.
Общая сумма выплат таким специалистам — 607,4 млн руб. Средний размер выплаты — от 24 тыс. до 252 тыс. руб. в зависимости от компании.
Количество специалистов, не согласившихся на раскрытие информации, — не менее 33 тыс. человек. Точное количество указать невозможно, поскольку из отчетности многих компаний нельзя сделать вывод, получил ли врач больше одной выплаты или нет.
Общая сумма выплат анонимным специалистам — 2,7 млрд руб. Средний размер выплаты — от 10 тыс. до 310 тыс. руб. в зависимости от компании.
Число врачей в 2018 году, по данным Росстата, — 560,2 тыс. человек.
Средняя по России ежемесячная зарплата врача, по данным Росстата, — 75 тыс. руб.
На сайте AIPM членами ассоциации указаны 63 компании (с учетом дочерних структур). Дедлайном при публикации материалов традиционно является 30 июня. По состоянию на 4 июля на сайтах компаний — членов AIPM были доступны лишь 43 отчета. Среди производителей, которые ранее раскрывали информацию, но в этом году в срок ее не предоставили, — Allergan (ее покупает AbbVie), AstraZeneca, Ferring Pharmaceutical, Merz Pharma, Zambon Group. На запросы РБК в этих компаниях на момент публикации не ответили.
Больше всего врачам в 2018 году перечислила немецкая Bayer — 498,6 млн руб. Количество медиков, получивших выплаты, может составлять от 3,9 тыс. до 7 тыс. человек. Конкретная информация приведена только в отношении 74 человек.
Наименьший размер выплат в 2018 году — 1,9 млн руб. — у американской Celgene. Деньги получили 24 специалиста, из которых лишь о семи информация раскрыта.
В 14 раз — с 3,1 млн до 44,2 млн руб. — в прошлом году выросли платежи у Amgen. В 2018 году эта американская компания сотрудничала с 498 врачами, известны имена 84 из них.
Больше всех снизился бюджет у французской Ipsen: с 471,2 млн руб. в 2017 году до 41,9 млн руб. в 2018-м. В прошлом году эти деньги получили не менее 583 специалистов, из них 558 разрешили опубликовать подробную информацию о своем вознаграждении.
За что фармкомпании платят врачам
Максимальные выплаты врачам представляют собой преимущественно вознаграждения за оказание услуг и консультирование, свидетельствуют проанализированные РБК отчеты.
За этой формулировкой может скрываться все что угодно: разработка протоколов исследований или, например, цикл лекций, указывает главный врач столичной Городской клинической больницы им. С.С.Юдина Денис Проценко. В основном такие выплаты от компаний — это не разовые отчисления, а гонорары за чтение лекций и участие в научных мероприятиях, которые проходят при поддержке фармкомпаний, объясняет заведующий отделением реанимации и интенсивной терапии московской Городской клинической больницы № 29 Алексей Эрлих.
Закон «Об основах охраны здоровья граждан в РФ» не разрешает медицинским работникам принимать денежные средства от фармкомпаний и их представителей. Но под этот запрет не попадают гонорары за проведение клинических исследований и испытаний и вознаграждения за педагогическую и научную деятельность.
Рейтинг врачей
По итогам 2018 года у 29 российских врачей размер платежей от фармкомпаний превысил 1 млн руб. Лидером рейтинга стала Татьяна Пестова, специалист-репродуктолог из Челябинска. От Merck за «оказанные услуги и консультирование» она в прошлом году получила почти 2,7 млн руб., еще 164 тыс. руб. (из них 102 тыс. — компенсация транспортных расходов) ей перечислила Abott. Связаться с Пестовой в пятницу, 5 июля, не удалось.
Главному внештатному эндокринологу министерства здравоохранения Краснодарского края Инне Кудлай та же Merck, как указано в ее отчете, перечислила за услуги и консультации 2,6 млн руб. Еще 7 тыс. руб. в качестве компенсаций транспортных расходов этот врач получила от Ipsen. Но в беседе с корреспондентом РБК Кудлай заявила, что вообще не работает ни с Merck, ни с Ipsen. «Я была бы очень рада, если бы была таким богатым человеком», — ответила Кудлай. Она перестала отвечать на звонки корреспондентов РБК после того, как ей были отправлены отчеты фармкомпаний.
Отказался комментировать заявленные в отчетности венгерской Egis почти 2,2 млн руб. директор терапевтический клиники и заведующий кафедрой терапии, клинической фармакологии и скорой медицинской помощи МГМСУ им. А.И.Евдокимова Аркадий Верткин.
Профессор кафедры молекулярной фармакологии РНИМУ им. Н.И.Пирогова Александр Духанин подтвердил РБК, что сотрудничал в прошлом году с Pfizer и Sanofi, и допустил, что мог получить выплаты и от других фармкомпаний. Но он усомнился с заявленном размере выплат: почти 78 тыс. руб. за оказанные услуги и консультации от Pfizer и 1,3 млн руб. (с учетом 332 тыс. руб. компенсации транспортных расходов) от Sanofi. «Предполагаю, что включены не только гонорары, но расходы на перелеты и проживание, потому что сумма получается какая-то астрономическая, — заявил Духанин. — Поскольку я преподаватель, научный сотрудник, а не практикующий врач, то эти суммы уходят на образовательную работу».
Кардиоревматолог профессор Илья Егоров (на личном сайте называет себя «постоянным медицинским экспертом» «Первого канала», «России 1», «ТВ Центра» и НТВ») рассказал, что для Egis он делает «буквально несколько выступлений в год», а для Merck — 10–12. Компании отчитались о перечисленных Егорову соответственно 723 тыс. и 1,3 млн руб. (из них 63 тыс. — компенсации транспортных расходов). В этих цифрах указан не только гонорар лектору, но и другие расходы, убежден Егоров.
«У фармкомпаний есть свой интерес — конечно, они приглашают лекторов, которые в своих выступлениях так или иначе будут говорить про их препараты. Но 20 лет назад, когда к нам только пришла эта форма бизнеса, это была чистая реклама, а потом стало понятно, что это неинтересно врачам, — вспоминает Егоров. — И в последнее десятилетие лекторы, которые работают с фармкомпаниями, понимают, что они должны дать своим слушателям вкусную, яркую, актуальную тему — обучение правильной диагностике, разговору с пациентом».
Сейчас реклама препаратов стала настолько непопулярной, настолько невостребованной, что о них говорится вскользь, в контексте, уверяет Егоров.
Связаться с другими фигурирующими в рейтинге врачами не удалось.

Подробнее на РБК:
https://www.rbc.ru/rbcfreenews/5d218f109a794781e30c6b93
Добро всегда накажет Зло, поставит его на колени и жестоко убьет.
-
 Андрей Эдельвейсс
Андрей Эдельвейсс
Автор темы - Трактирщик
- Сообщения: 8358
- Зарегистрирован: 29 май 2015, 19:55
- Награды: 5
- Откуда: СССР
- Род занятий: колымим
- :




- Благодарил (а): 1099 раз
- Поблагодарили: 2392 раза
- Status: Не в сети

Роспотребнадзор объяснил, кому и в каких случаях опасно носить медицинские маски. Это может привести к болезням.
Медицинские маски эффективны, если их носит инфицированный человек, но в ряде случаев эффект от них может быть губительным, сообщили в Роспотребнадзоре.
По словам экспертов, медицинская маска защищает только на 80%, препятствуя распространению аэрозоля, образующегося при дыхании и разговоре. Этот аэрозоль может содержать вирус SARS-CoV-2, объяснили специалисты. Но 100-процентной гарантии, что не заразишься, нет.
Как уточнили в Роспотребнадзоре, прогулки и занятия спортом в масках могут причинить человеку вред, если он страдает хроническими заболеваниями или имеет противопоказания к высокой физической активности, пишет ФАН.
Напомним, еще в марте во Всемирной организации здравоохранения однозначно заявляли: носить маску здоровым людям не нужно. Там подчеркивали, что свидетельств того, что систематическое использование медицинских масок здоровыми людьми позволяет предотвратить передачу вируса 2019-nCoV, нет. Что касается ношения маски на улице — то надевать ее "большая ошибка", подчеркивали в ВОЗ.
"На открытом воздухе вирусы и так быстро гибнут. А маска при ходьбе ограничивает доступ кислорода, могут начаться головокружение, одышка", — предупреждали эксперты ВОЗ.
Ольга Толмачева
Медицинские маски эффективны, если их носит инфицированный человек, но в ряде случаев эффект от них может быть губительным, сообщили в Роспотребнадзоре.
По словам экспертов, медицинская маска защищает только на 80%, препятствуя распространению аэрозоля, образующегося при дыхании и разговоре. Этот аэрозоль может содержать вирус SARS-CoV-2, объяснили специалисты. Но 100-процентной гарантии, что не заразишься, нет.
Как уточнили в Роспотребнадзоре, прогулки и занятия спортом в масках могут причинить человеку вред, если он страдает хроническими заболеваниями или имеет противопоказания к высокой физической активности, пишет ФАН.
Напомним, еще в марте во Всемирной организации здравоохранения однозначно заявляли: носить маску здоровым людям не нужно. Там подчеркивали, что свидетельств того, что систематическое использование медицинских масок здоровыми людьми позволяет предотвратить передачу вируса 2019-nCoV, нет. Что касается ношения маски на улице — то надевать ее "большая ошибка", подчеркивали в ВОЗ.
"На открытом воздухе вирусы и так быстро гибнут. А маска при ходьбе ограничивает доступ кислорода, могут начаться головокружение, одышка", — предупреждали эксперты ВОЗ.
Ольга Толмачева
Добро всегда накажет Зло, поставит его на колени и жестоко убьет.
Кто сейчас на конференции
Сейчас этот форум просматривают: Claude [Bot] и 0 гостей